
下表为元素周期表的一部分:
| 族 周期 | | | | |||||
| 1 | ① | | | | | | | |
| 2 | | | | | | ② | | |
| 3 | ③ | | | ④ | | ⑤ | ⑥ | |
(14分)
Ⅰ.(1)第四周期第ⅣA族(1分)
(2)Na>S>O(2分)
(3)HCl>H2S>SiH4(2分)
(4)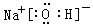 或
或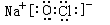 (2分)
(2分)
Ⅱ.(1)2Na2O2 +2H2O = 4Na+ + 4OH― + O2↑(2分)
(2)NaHSO3(1分)
c(Na+)> c(HSO3-) > c(H+) > c(SO32-) > (OH-)(2分)
(3)2SO2 +O2 2SO3(2分)
2SO3(2分)
解析试题分析:根据元素所在周期表中的位置,可知元素的种类,①为H元素,②为O元素,③为Na元素,④为Si元素,⑤为S元素,⑥为Cl元素,
Ⅰ.⑴④为Si元素,在周期表中的位置第四周期第ⅣA族;答案:第四周期第ⅣA族。
⑵电子层越多半径越大,电子层数一样的,质子数越小,半径越大,③为Na元素,⑤为S元素,同一周期,Na>S,②为O元素,⑤为S元素,同一主族,S>O,②、③、⑤的原子半径由大到小的顺序为:Na>S>O,答案:Na>S>O;
⑶同周期元素从左到右元素的非金属性逐渐增强,同主族元素从上到下元素的非金属性逐渐减弱,元素的非金属性越强,对应氢化物越稳定,Cl、S、Si,同一周期,所以④、⑤、⑥的气态氢化物的稳定性由强到弱的顺序是:HCl>H2S>SiH4;答案:HCl>H2S>SiH4;
⑷H、O、Na、Cl中的某些元素可形成既含离子键又含极性共价键的化合物有多种:如:NaOH、NaClO等,电子式为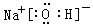 或
或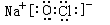 ,答案:
,答案: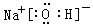 或
或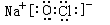 。
。
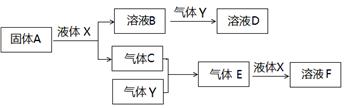
Ⅱ.A是一种淡黄色固体,A是Na2O2,气体Y是一种大气污染物,直接排放会形成酸雨,Y为SO2,推出:A、Na2O2 B、NaOH C、O2 D、NaClO E、SO3 F、H2SO4 X、H2O Y、SO2
(1)Na2O2和水反应:2Na2O2 +2H2O = 4Na+ + 4OH― + O2↑答案:2Na2O2 +2H2O = 4Na+ + 4OH― + O2↑;
(2)当NaOH与SO2物质的量之比为1:1且恰好完全反应时,NaOH+SO2=NaHSO3,所得溶液D的溶质为NaHSO3,HSO3―的电离多于水解,所以溶液呈酸性,溶液中各种离子浓度由大到小的顺序为:c(Na+)> c(HSO3-) > c(H+) > c(SO32-) > (OH-),答案:NaHSO3、c(Na+)> c(HSO3-) > c(H+) > c(SO32-) > (OH-)
(3)气体SO2与气体O2反应的化学方程式 ;2SO2 +O2 2SO3,答案:2SO2 +O2
2SO3,答案:2SO2 +O2 2SO3。
2SO3。
考点:元素周期律和元素周期表的综合应用,无机推断


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题
在一定条件下,单质B、C、D、E都能与A单质发生化合反应,转化关系如图所示。已知:①G是黑色晶体,能吸附B单质;②H能与氢氧化钠溶液或盐酸反应;③实验时在G和C的混合物表面加入某强氧化剂粉末,在表面上插入一根除去氧化膜的E片,点燃E引发G与C的反应;④I是绿色植物光合作用的原料,温室中常用它作肥料。根据上述信息,回答下列问题: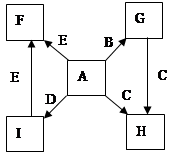

(1)I的电子式为 ,G的俗名是 。
(2)以C和E为电极在NaOH溶液中构成原电池,该原电池的负极反应式为 。
(3)根据E和A反应的能量变化图像写出热化学方程式: 。
(4)两种常见含C元素的盐,一种pH>7,另一种pH<7,写出这两种溶液混合时发生反应的离
子方程式:
(5)写出B在高温下和水蒸气反应的化学方程式并标出电子转移方向和总数 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
A、B、C、D均为中学化学常见物质,且含有一种相同的元素,它们之间有如下转化关系,其中A是单质。
(1)若A是一种淡黄色固体,B是气态氢化物,C、D为气态氧化物,且C是形成酸雨的主要物质。请写出C与B反应的化学方程式_________________________________。
(2)若B是气态氢化物,C、D为气态氧化物,且C、D是形成光化学烟雾的一个重要原因。请写出反应③的化学方程式____________________________________。实验室中检验气体B存在用的试剂或用品为________________。
(3)若B、D既能溶于强酸溶液,又能溶于强碱溶液,反应②③均需要强碱性溶液,反应④可以通过滴加少量稀盐酸实现。据此判断A元素在周期表中的位置是_________________。请写出②的离子方程式_____________________________________________________________________________。
(4)若C是一种淡黄色固体,常用于吸吸面具中的供氧剂,D是一种强碱。写出反应④的离子方程式
_____________________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
A、B、C、D、E为五种元素的单质,其余为化合物。其中只有E为金属元素,五种元素的原子序数按B、D、C、A、E顺序依次增大,D、C元素在周期表中位置相邻,在一定条件下,B分别和A、C、D化合生成甲、乙、丙,乙、丙每个分子中均含有10个电子;C和D化合可得丁。各物质相互转化关系如下图: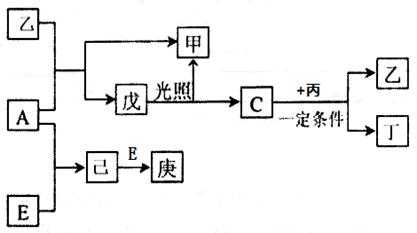
请回答下列问题:
(1)写出E元素在周期表的位置 。
(2)戊的名称为_________________;用途 (只写一种)。
(3)写出实验室制取A反应的离子方程式_________________________________。
(4)常温下A与足量的丙发生反应生成单质D,写出该反应的化学方程式
____________________________________________________________________。
(5)写出足量E和稀硝酸反应的化学方程式:
_______________________________________________________________________。
(6)实验室配制庚溶液的方法是______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
已知通常状况下甲、乙、丙、丁等为气体单质,A、B、C、D、E、F、G、H等为化合物,其中A、B、E、G均为气体,C为常见液体。反应①、②、③都是重要的化工反应,反应④是重要的实验室制取气体的反应。有关的转化关系如下图所示(反应条件均已略去)。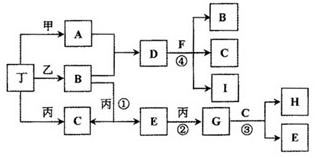
请回答下列问题:
(1)反应④的化学方程式为: ________________________。
(2)B和E在一定条件下可发生反应,这是一个具有实际意义的反应,可消除E对环境的污染,该反应氧化产物与还原产物的物质的量之比为________。
(3)0.1mol lL-1A溶液和0.1mol ?L-1B溶液等体积混合,溶液呈________性,原因是(用离子方程式说明) ________________。
(4)请设计实验检验D晶体中的阳离子(简述实验操作、现象和结论):________________。
(5)pH相同的A、D、H三种溶液,由水电离出的c(OH-)的大小关系是(用A、D、H表示) : ____________。
(6)向一定量的Fe、FeO、Fe3O4的混合物中,加入1mol? L-1 A的溶液100 mL,恰好使混合物全部溶解,且放出336mL(标准状况下)的气体,向所得溶液中加入KSCN溶液,溶液无红色出现;若取同质量的Fe、FeO、Fe3O4混合物,加入1 mol ? L-1 H的溶液,也恰好使混合物全部溶解,且向所得溶液中加入KSCN溶液,溶液也无红色出现,则所加入的H溶液的体积是________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下图表示某些化工生产的流程(部分反应条件和产物略去)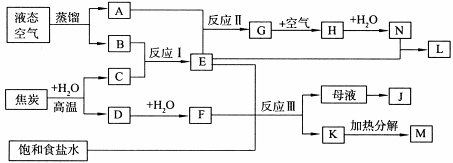
(1)反应Ⅰ需在500℃进行,其主要原因是 。
(2)G转化为H的过程中,需要不断补充空气,其原因是 。
(3)写出反应Ⅲ的化学方程式 。
(4)工业上,向析出K的母液中通氨气,加入细小食盐颗粒,冷却后可析出副产品。通入氨气的作用是 (填序号)。
a.增大NH+4的浓度,使J更多地析出
b.使K更多地析出
c.使K转化为M,提高析出的J的纯度
(5)写出上述流程所涉及的化学工业的名称 。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列反应中,反应后固体物质增重的是
| A.氢气通过灼热的CuO粉末 | B.二氧化碳通过Na2O2粉末 |
| C.铝与Fe2O3发生铝热反应 | D.将锌粒投入Cu(NO3)2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列过程中,没有发生化学变化的是( )
| A.干冰用于人工降雨 |
| B.蔗糖中加入浓硫酸,蔗糖变黑,体积膨胀 |
| C.溶洞中钟乳石的形成 |
| D.豆科作物的根瘤菌对空气中氮的固定 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关实验或操作的叙述正确的是( )
| A.用图1所示的装置做喷泉实验时观察到产生白色喷泉 |
| B.如图2所示的两套装置均可制备NH3(不考虑净化和收集) |
| C.称取2.5 g CuSO4·5H2O,放入100 mL容量瓶中,配制0.10 mol·L-1CuSO4溶液 |
| D.除去NaHCO3溶液中的Na2CO3,可加入Ca(OH)2溶液后过滤 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com