

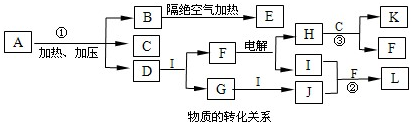
 CO (NH2)2+H2O.再从NH3→G→J的变化均加入同一种物质I引起,故而判断出I为O2.进而推出F为H2O,H为H2,L为HNO3.推断物质为:A、CO (NH2)2;B、C3H6N6;C、CO2;D、NH3;F、H2O;G、NO;H、H2;I、O2;L、HNO3;J、NO2;K、CH4;依据判断出的各物质分析判断回答;
CO (NH2)2+H2O.再从NH3→G→J的变化均加入同一种物质I引起,故而判断出I为O2.进而推出F为H2O,H为H2,L为HNO3.推断物质为:A、CO (NH2)2;B、C3H6N6;C、CO2;D、NH3;F、H2O;G、NO;H、H2;I、O2;L、HNO3;J、NO2;K、CH4;依据判断出的各物质分析判断回答; CO (NH2)2+H2O.再从NH3→G→J的变化均加入同一种物质I引起,故而判断出I为O2.进而推出F为H2O,H为H2,L为HNO3.推断物质为:A、CO (NH2)2;B、C3H6N6;C、CO2;D、NH3;F、H2O;G、NO;H、H2;I、O2;L、HNO3;J、NO2;K、CH4;
CO (NH2)2+H2O.再从NH3→G→J的变化均加入同一种物质I引起,故而判断出I为O2.进而推出F为H2O,H为H2,L为HNO3.推断物质为:A、CO (NH2)2;B、C3H6N6;C、CO2;D、NH3;F、H2O;G、NO;H、H2;I、O2;L、HNO3;J、NO2;K、CH4; CO (NH2)2+H2O;
CO (NH2)2+H2O; ;
;
 H3O++OH-,通过类比不难得出液态NH3电离方程式为:2NH3
H3O++OH-,通过类比不难得出液态NH3电离方程式为:2NH3  NH4++NH2-. 故答案为:2NH3
NH4++NH2-. 故答案为:2NH3  NH4++NH2-;
NH4++NH2-; N2(g)+2H2O(g);△H=-568kJ/mol.
N2(g)+2H2O(g);△H=-568kJ/mol. N2(g)+2H2O(g);△H=-568kJ/mol
N2(g)+2H2O(g);△H=-568kJ/mol

 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:阅读理解


 NH4++NH2-
NH4++NH2- NH4++NH2-
NH4++NH2-查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源:江山市模拟 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:

(1)若X由M、N两种短周期且同周期元素组成,M原子的最外层电子数是最内层电子数的![]() ,N元素最高价与它的负价代数和为6。
,N元素最高价与它的负价代数和为6。
①写出反应Ⅱ的离子方程式______________________________。
②下图为反应Ⅳ达平衡后改变反应条件,反应速率随时间变化的情况,已知t2—t3阶段为使用催化剂;t3—t4阶段为减小体系的压强,写出符合上述条件的化学方程式___________________(写一个即可,用具体物质表示);若t4—t5阶段为升高体系的温度,则该反应为___________________(填“放热”或“吸热”)。

③某温度下,四个容器中均进行着上述反应,各物质的物质的量浓度及正逆反应速率关系如下表所示。请填写表中相应的空格。
容器编号 | c(C)/mol·L-1 | c(D)/mol·L-1 | c(G)/mol·L-1 | v正、v逆比较 |
甲 | 0.06 | 0.60 | 0.60 | v正=v逆 |
乙 | 0.06 | 0.50 | 0.40 |
|
丙 | 0.12 | 0.40 | 0.80 | v正<v逆 |
丁 | 0.12 | 0.30 |
| v正=v逆 |
(2)若X是一种含氧酸盐,B是金属单质,C、D是非金属单质,反应Ⅱ需要B与A的浓溶液共热才能进行,且生成的E与G是同一种物质。写出反应Ⅰ的化学方程式___________________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com