
| A、乙烯使溴水或酸性高锰酸钾褪色均属于加成反应 |
| B、用乙醇与浓硫酸加热至170℃制乙烯的反应属于取代反应 |
| C、用重铬酸钾溶液检验司机是否酒驾所发生的反应属于乙醇的氧化反应 |
| D、用“地沟油”生产生物柴油只发生酯化反应 |


科目:高中化学 来源: 题型:
 甲、乙、丙为初中化学常见物质,其中乙为胃液中的一种酸.他们相互转化关系如图所示(“→”表示物质变化,部分反应条件和部分生成物已省略).
甲、乙、丙为初中化学常见物质,其中乙为胃液中的一种酸.他们相互转化关系如图所示(“→”表示物质变化,部分反应条件和部分生成物已省略).查看答案和解析>>
科目:高中化学 来源: 题型:
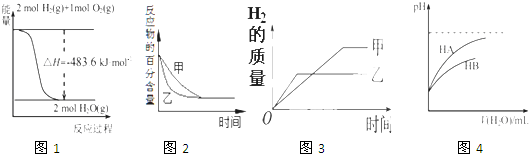
| A、图1表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为241.8 kJ?mol-1 |
| B、图2表示压强对可逆反应2A(g)+2 B(g)?3C(g)+D(s)的影响,乙的压强比甲的压强大 |
| C、图3表示等质量的钾、钠分别与足量水反应,则甲为钠 |
| D、图4表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则相同条件下NaA溶液的pH大于同浓度的NaB溶液的pH |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、与A属于同类化合物的同分异构体只有2种 |
| B、A在一定条件下可与4 mol H2发生加成反应 |
| C、A分子属于酯类化合物,在一定条件下不能发生水解反应 |
| D、符合题中A分子结构特征的有机物只有1种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、土壤中含有铁粉、二氧化锰等 |
| B、黑砖瓦是煅烧过程中附着了炭黑,红砖则是添加了红色耐高温染料 |
| C、土壤中含有的铜元素经过不同工艺煅烧,分别生成了黑色CuO和红色Cu或Cu2O |
| D、土壤中含有的铁元素经过不同工艺煅烧,分别生成了黑色Fe304或FeO和红色Fe2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若混合后溶液中c(Na+)>c(X-),说明HX的电离程度弱于X-的水解程度 |
| B、若混合溶液呈酸性,则c(X-)>c(Na+)>c(HX)>c(H+)>c(OH-) |
| C、混合溶液中c(HX)+c(X-)=0.2 mol?L-1 |
| D、混合溶液中c(Na+)+c(H+)=c(X-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
 在t℃时,AgBr在水中的沉淀溶解平衡曲线如图所示.又知t℃时AgCl的Ksp=4×10-10,下列说法不正确的是( )
在t℃时,AgBr在水中的沉淀溶解平衡曲线如图所示.又知t℃时AgCl的Ksp=4×10-10,下列说法不正确的是( )| A、如图中a点对应的是AgBr的不饱和溶液 |
| B、在t℃时,Ksp(AgBr)=4.9×10-13 |
| C、在t℃时,AgCl(s)+Br-(aq)?AgBr(s)+Cl-(aq)的平衡常数K≈816 |
| D、在AgBr的饱和溶液中加入NaBr固体,可使溶液由b点到以c点 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③⑤ | B、①③④⑤ |
| C、②③⑤ | D、②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com