
| A. | 溶液中由水电离的氢离子浓度为10-4 | |
| B. | 与pH=4的盐酸等体积混合后,c(Cl-)>c(NH4+) | |
| C. | 通入一定量氨气后,依然存在c(NH4+)+c(H+)=c(OH-) | |
| D. | 氨水中存在:c(NH3•H2O)>c(NH4+)>c(OH-)>c(H+) |
分析 A、对pH=10,溶液中的氢离子全部由水电离产生的,所以氢离子浓度为10-10;
B、pH=4的盐酸等体积混合后溶液呈碱性,根据电荷守恒分析解答;
C、电荷守恒分析解答;
D、溶液中存在水的电离,所以氢氧根离子浓度大于铵根离子.
解答 解:A、对pH=10的氨水而言,溶液中的氢离子全部由水电离产生的,所以氢离子浓度为10-10,故A错误;
B、pH=4的盐酸等体积混合后溶液呈碱性,所以c(OH-)>c(H+),根据电荷守恒:c(Cl-)+c(OH-)=c(NH4+)+c(H+),所以c(Cl-)<c(NH4+),故B错误;
C、电荷守恒:c(NH4+)+c(H+)=c(OH-),故C正确;
D、溶液中存在水的电离,所以氢氧根离子浓度大于铵根离子,所以离子浓度为:c(NH3•H2O)>c(OH-)>c(NH4+)>c(H+),故D错误;
故选C.
点评 本题考查了水的电离及其影响因素和离子浓度大小的比较,题目难度中等,注意电荷守恒在解题中的应用.


科目:高中化学 来源: 题型:多选题

| A. | 氯气 | B. | ClO2 | C. | NaCl | D. | NaClO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分别对两溶液微热时,K均增大、溶液pH均减小 | |
| B. | 恒温下分别稀释两溶液时,K均不变、溶液pH均增大 | |
| C. | 25℃时a+b=14 | |
| D. | 25℃时两溶液混合所得pH=8的溶液中,c(X-)>c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④⑤ | B. | ②④⑥ | C. | ①③④ | D. | ②④⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定条件下,2molSO2和1molO2混合在密闭容器中充分反应后容器中的分子数大于2NA | |
| B. | 0.1mol铁粉与足量水蒸气反应生成的H2分子数目为0.1NA | |
| C. | 由1molCH3COONa和少量CH3COOH形成的中性溶液中,CH3COO-数目为NA个 | |
| D. | 分子数目为0.1NA的N2和NH3混合气体,原子间含有的共用电子对数目为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
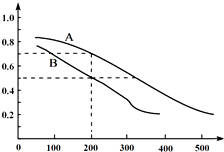 科学家开发出一种“洁净煤技术”,通过向地下煤层“气化炉”中交替鼓入空气和水蒸气的方法,连续产出高热值的煤炭气,其主要成分是CO和H2.“气化炉”中主要反应有:
科学家开发出一种“洁净煤技术”,通过向地下煤层“气化炉”中交替鼓入空气和水蒸气的方法,连续产出高热值的煤炭气,其主要成分是CO和H2.“气化炉”中主要反应有:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com