
| A、在硅酸钠溶液中滴加酚酞 |
| B、碳酸钠溶液中滴加酚酞 |
| C、硫酸铁溶液中滴加硫氰化钾溶液 |
| D、碳酸氢钠溶液中滴加稀盐酸 |


科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
| C、(A-N+2)mol | ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:


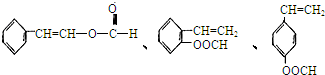 、
、查看答案和解析>>
科目:高中化学 来源: 题型:
 被誉为中国“新四大发明”之一的复方蒿甲醚是第一个由中国发现的全新化学结构的药品,也是目前在国际上获得广泛认可的中国原创药品.其主要成分是青蒿素(一种从青蒿中分离得到的具有新型化学结构的抗疟药),其结构简式如下图所示.下列有关该有机物的叙述正确的是( )
被誉为中国“新四大发明”之一的复方蒿甲醚是第一个由中国发现的全新化学结构的药品,也是目前在国际上获得广泛认可的中国原创药品.其主要成分是青蒿素(一种从青蒿中分离得到的具有新型化学结构的抗疟药),其结构简式如下图所示.下列有关该有机物的叙述正确的是( )| A、该有机物的分子式为C14H23O5 |
| B、该有机物不能与NaOH溶液反应 |
| C、该有机物分子中含有过氧键,一定条件下具有氧化性 |
| D、该有机物易溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、Na+、AlO2-、NO3- |
| B、NH4+、Al3+、NO3-、SO42- |
| C、K+、NH4+、SO32-、S2- |
| D、K+、Ag+、NO3-、Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:
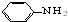 +CH3COOH
+CH3COOH| △ |
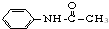 +H2O
+H2O| 名称 | 式量 | 性状 | 密度/g/cm3 | 沸点/℃ | 溶解度 | |
| 苯 胺 | 93 | 无色油状液体, 具有还原性 | 1.02 | 184.4 | 微溶于水 | 易溶于乙醇、乙醚等 |
| 乙 酸 | 60 | 无色液体 | 1.05 | 118.1 | 易溶于水 | 易溶于乙醇、乙醚 |
| 乙酰苯胺 | 135 | 白色晶体 | 1.22 | 304 | 微溶于冷水, 溶于热水 | 易溶于乙醇、乙醚 |
 注:刺形分馏柱的作用相当于二次蒸馏,用于沸点差别不太大的混合物的分离
注:刺形分馏柱的作用相当于二次蒸馏,用于沸点差别不太大的混合物的分离查看答案和解析>>
科目:高中化学 来源: 题型:
| A、有氨水可以鉴别MgCl2溶液和AlCl3溶液 |
| B、可以用澄清的石灰水鉴别SO2和CO2 |
| C、SO2能使FeCl3、KMnO4水溶液褪色 |
| D、金属钠与CuSO4溶液反应能析出单质Cu |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com