
| A. | 1.0 mol•L-1的KNO3溶液:H+、Fe2+、Cl-、SO42- | |
| B. | 饱和氯水中:NH4+、SO32-、AlO2-、Cl- | |
| C. | 与铝反应产生大量氢气的溶液:Na+、K+、CO32-、NO3- | |
| D. | c(H+)=1.0×10-13mol/L溶液中:K+、Na+、CH3COO-、Br- |
分析 A.离子之间发生氧化还原反应;
B.氯水含氧化性物质;
C.与铝反应产生大量氢气的溶液,为非氧化性酸或强碱溶液;
D.c(H+)=1.0×10-13mol/L溶液,显碱性.
解答 解:A.H+、Fe2+、NO3-发生氧化还原反应,不能共存,故A不选;
B.氯水含氧化性物质,与SO32-发生氧化还原反应,且氯水显酸性不能大量存在AlO2-,不能共存,故B不选;
C.与铝反应产生大量氢气的溶液,为非氧化性酸或强碱溶液,酸溶液中不能大量存在CO32-,且Al、H+、NO3-发生氧化还原反应不生成氢气,故C不选;
D.c(H+)=1.0×10-13mol/L溶液,显碱性,该组离子之间不反应,可大量共存,故D选;
故选D.
点评 本题考查离子共存,为高频考点,把握习题中的信息、离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意氧化还原反应及复分解反应的判断,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 葡萄糖 | B. | 乙酸 | C. | 蛋白质 | D. | 脂肪 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 海带中碘元素检验的实验过程是灼烧→溶解→过滤→萃取 | |
| B. | 用容量瓶配制一定物质的量浓度溶液时,加入蒸馏水需要用玻璃棒引流加至刻度线 | |
| C. | 用有机溶剂苯萃取碘水中的碘,分液时,有机层从分液漏斗的下口放出 | |
| D. | 用新制备的Cu(OH)2的悬浊液来鉴别乙醇、乙酸和葡萄糖三种无色溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
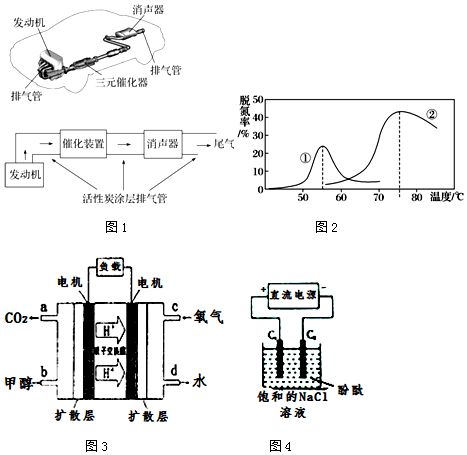
 甲醇是一种优质燃料,在工业上常用
甲醇是一种优质燃料,在工业上常用查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X、Y、Z三种元素中的两种或三种只能生成2种18电子的分子 | |
| B. | Z2X4可作为火箭发动机的燃料 | |
| C. | WX2中只含离子键 | |
| D. | Z的氢化物比Y的氢化物更稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验操作 | 实验目的 | |
| A | 将SO2通入紫色石蕊溶液中 | 证明SO2具有酸性和漂白性 |
| B | 用pH试纸测定NaHSO3溶液的pH | 比较HSO3-电离程度和水解程度的大小 |
| C | 溴乙烷与NaOH乙醇溶液共热,将得到的气体通入溴的四氯化碳溶液 | 证明反应得到的气体含有乙烯 |
| D | 向含酚酞的Na2SO3溶液中加入BaC12溶液 | 证明Na2SO3溶液中存在水解平衡 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤ | B. | ①③⑥ | C. | ④⑤⑦ | D. | ②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 卤代烷水解时,从氟到碘,由于非金属性依次减弱,所以水解越来越困难 | |
| B. | 溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+═AgBr↓ | |
| C. | 相同碳原子数的多卤代烃,随着卤原子数的增多,密度依次降低 | |
| D. | 常温下,CH3Cl是气体,甲烷的其他3种氯代产物都是液体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com