
| 甲 | 乙、丙、丁 | |
| ① | 常见干燥剂 | 浓硫酸、石灰石、碱石灰 |
| ② | 常见合金 | 不锈钢、青铜、生铁 |
| ③ | 腐蚀品 | 浓硫酸、烧碱、硝酸 |
| ④ | 碱性氧化物 | 过氧化钠、氧化镁、氧化铁 |
| ⑤ | 弱电解质 | 醋酸、一水合氨、水 |
| A. | ①② | B. | ③④⑤ | C. | ②③⑤ | D. | ①④⑤ |
分析 ①能够吸收水的物质可以用作干燥剂;
②合金是指由一种金属与其它金属或非金属熔合而成的具有金属特性的物质;
③浓硫酸、烧碱、硝酸都为强酸或者强碱,都具有很强的腐蚀性;
④碱性氧化物是和酸反应生成盐和水的氧化物,反应为复分解反应;
⑤水溶液中部分电离的电解质为弱电解质.
解答 解:①浓硫酸具有吸水性,可以用作干燥剂;石灰石不能用作干燥剂,碱石灰固体可用作干燥剂,故①错误;
②不锈钢、青铜、生铁是金属与其它金属或非金属熔合而成的具有金属特性的物质,都是合金,故②正确;
③浓硫酸、烧碱和硝酸都具有很强的腐蚀性,属于腐蚀品,故③正确;
④氧化镁、氧化铁与酸反应生成盐和水,属于碱性氧化物,而过氧化钠与酸反应生成盐和水外,还生成了氧气,所以过氧化钠不属于碱性氧化物,故④错误;
⑤醋酸、一水合氨、水都在水溶液中存在电离平衡,属于弱电解质,故⑤正确;
故选C.
点评 本题考查了常见的干燥剂、合金、和碱性氧化物、弱电解质概念判断及各种物质的成分掌握,题目难度中等.


科目:高中化学 来源: 题型:选择题
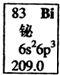
| A. | Bi元素的质量数是209 | |
| B. | Bi元素的相对原子质量是209.0 | |
| C. | Bi原子6p能级有一个未成对电子 | |
| D. | Bi原子最外层有5个能量相同的电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
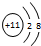 ,F中的化学键为离子键、共价键;
,F中的化学键为离子键、共价键; ; F和AB2反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2;
; F和AB2反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2;查看答案和解析>>
科目:高中化学 来源: 题型:填空题
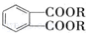 (代号DMP)是一种常用的酯类塑化剂,其蒸气对氢气的相对密度为97.工业上生产DMP的流程如图所示:
(代号DMP)是一种常用的酯类塑化剂,其蒸气对氢气的相对密度为97.工业上生产DMP的流程如图所示: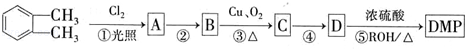
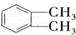 的名称1,2-二甲苯(或邻二甲苯),D中官能团的名称为醛基,DMP的分子式为C10H10O4.
的名称1,2-二甲苯(或邻二甲苯),D中官能团的名称为醛基,DMP的分子式为C10H10O4.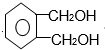 +O2$→_{△}^{Cu}$
+O2$→_{△}^{Cu}$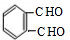 +2H2O.
+2H2O.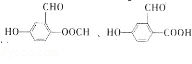 .
.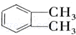 制备DMP的另一种途径:
制备DMP的另一种途径: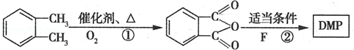
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 都只由C、H、O三种元素组成 | B. | 都是食物中的基本营养物质 | ||
| C. | 都能发生水解反应 | D. | 都属于高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲状腺机能亢进 | B. | 佝偻病 | C. | 地方性甲状腺肿 | D. | 雄性激素减少 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
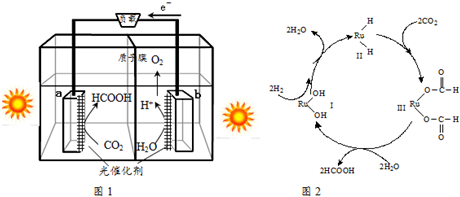
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com