
【题目】三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42﹣可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室.下列叙述正确的是( ) 
A.通电后中间隔室的SO42﹣离子向正极迁移,正极区溶液pH增大
B.该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品
C.负极反应为2H2O﹣4e﹣=O2+4H+ , 负极区溶液pH降低
D.当电路中通过1mol电子的电量时,会有0.5mol的O2生成
【答案】B
【解析】解:A、阴离子向阳极(即正极区)移动,氢氧根离子放电pH减小,故A错误;B、直流电场的作用下,两膜中间的Na+和SO42﹣可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室,通电时,氢氧根离子在阳极区放电生成水和氧气,考虑电荷守恒,两膜中间的硫酸根离子会进入正极区,与氢离子结合成硫酸;氢离子在阴极得电子生成氢气,考虑电荷守恒,两膜中间的钠离子会进入负极区,与氢氧根离子结合成氢氧化钠,故可以得到NaOH和H2SO4产品,故B正确;
C、负极即为阴极,发生还原反应,氢离子得电子生成氢气,故C错误;
D、每生成1mol氧气转移4mol电子,当电路中通过1mol电子的电量时,会有0.25mol的O2生成,故D错误.
故选B.
A、阴离子向阳极(即正极区)移动,氢氧根离子放电pH减小;
B、从两极的电极反应和溶液的电中性角度考虑;
C、负极即为阴极,发生还原反应,氢离子放电;
D、当电路中通过1mol电子的电量时,会有0.25mol的O2生成.


 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:
【题目】向饱和澄清石灰水中加入少量CaC2,充分反应后恢复到原来的温度,所得溶液中
A.c(Ca2+)、c(OH-)均增大B.c(Ca2+)、c(OH-)均保持不变
C.c(Ca2+)、c(OH-)均减小D.c(OH-)增大、c(H+)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某可逆反应mA(g)+nB(g)pC(g),在密闭容器中进行,如图表示在不同反应时间t、温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线,由曲线分析,下列判断正确的是( ) 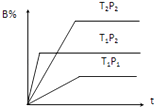
A.T1<T2、P1>P2、m+n>p,△H<0
B.T1>T2、P1<P2、m+n>p,△H>0
C.T1>T2、P1<P2、m+n<p,△H>0
D.T1<T2、P1>P2、m+n<p,△H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( ) 
A.Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如图一所示,石墨电极上产生氢气,铜电极发生氧化反应
B.图一所示当有0.1mol电子转移时,有0.1mol Cu2O生成
C.图二装置中发生:Cu+2Fe3+═Cu2++2Fe2+ , X极是负极,Y极材料可以是铜
D.如图二,盐桥的作用是传递电荷以维持电荷平衡,Fe3+经过盐桥进入左侧烧杯中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)将稀盐酸逐滴滴入到含有酚酞的NaOH溶液中,可观察到的现象是 , 反应的离子方程式为:
(2)若适量的N2和O2完全反应,每生成23g NO2需要吸收16.95kJ热量.其热化学方程式为
(3)已知C的燃烧热△H=﹣393.5kJ/mol,则24g C在O2中完全燃烧生成CO2(g)放出的热量为kJ.
(4)工业上常用天然气作为制备CH3OH的原料.已知:
①CH4(g)+O2(g)=CO(g)+H2(g)+H2O(g)△H=﹣321.5kJ/mol
②CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+250.3kJ/mol
③CO(g)+2H2(g)=CH3OH(g)△H=﹣90.0kJ/mol
CH4(g)与O2(g)反应生成CH3OH(g)的热化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氟化氮(NF3)是一种无色、无味的气体,它是微电子工业技术的关键原料之一,可由氨气和氟气反应得到:4NH3+3F2═NF3+3NH4F.在潮湿的空气中,NF3能与水蒸气发生氧化还原反应,其反应的产物有HF、NO和HNO3 . 下列说法正确的是( )
A.制取NF3的反应中,氧化剂与还原剂的物质的量之比为3:1
B.在NF3与H2O的反应中,H2O作还原剂
C.若在制取NF3的反应中有0.5 mol NH3参加反应,转移电子的物质的量为3 mol
D.NF3在空气中一旦泄漏,不易于发现
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室以一种工业废渣(主要成分为MgCO3、MgSO4和少量Fe、Al的氧化物)为原料制备MgCO33H2O.实验过程如图1 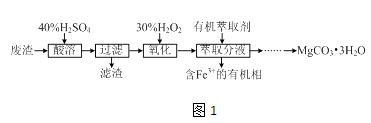
(1)酸溶需加热的目的是;过滤时用到的玻璃仪器有
(2)加入H2O2氧化时发生发应的离子方程式为 .
(3)用如图2所示的实验装置进行萃取和分液,以除去溶液中的Fe3+ . 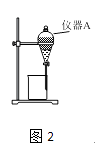
①实验装置图2中仪器A的名称为 .
②为使Fe3+尽可能多地从水相转移至有机相,采取的操作:向装有溶液的仪器A中加入一定量的有机萃取剂,、静置、分液,并重复多次.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】火药是中国古代四大发明之一,由硫磺、火硝和木炭粉均匀混合而成,点燃后可能发生的反应:S+2KNO3+3C=N2↑+3CO2↑+X(已配平),则物质X是
A. K2S B. SO2 C. H2S D. SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向铁铜合金中加入过量的硝酸溶液,得到NO2、N2O4、NO混合气体,向反应后溶液中加入2mol/LNaOH溶液,至沉淀恰好完全.若将得到的NO2、N2O4、NO混合气体,与2.24L(标准状况下)O2混合后通入水中恰好被完全吸收生成硝酸.则反应中消耗的NaOH溶液的体积是( )
A.150ml
B.180ml
C.200ml
D.250ml
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com