
下列关于化学反应速率的说法正确的是
| A.化学反应速率是指单位时间内任何一种反应物物质的量的减少或任何一种生成物物质的量的增加 |
| B.化学反应速率为0.8 mol /(L·s)是指1s 时某物质的浓度为0.8mol/L |
| C.根据化学反应速率的大小可以知道化学反应进行的快慢 |
| D.决定反应速率的主要因素是反应物的浓度 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:单选题
碘钨灯比白炽灯使用寿命长。灯管内封存的少量碘与使用过程中沉积在管壁上的钨可以发生反应:W(s)+I2(g)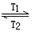 WI2(g) ΔH<0(温度T1<T2)。下列说法正确的是
WI2(g) ΔH<0(温度T1<T2)。下列说法正确的是
| A.灯管工作时,扩散到灯丝附近高温区的WI2(g)会分解出W,W重新沉积到灯丝上 |
| B.灯丝附近温度越高,WI2(g)的转化率越低 |
C.该反应的平衡常数表达式是 |
| D.利用该反应原理可以提纯钨 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
对于100mL 1mol/L盐酸与锌粒的反应,采取下列措施能使反应速率加快的是( )
①升高温度;②改用100mL 3mol/L盐酸;③多用300mL 1mol/L盐酸;④用等量锌粉代替锌粒;⑤滴入少量CuSO4溶液
| A.①③④⑤ | B.①②④⑤ | C.①②③④ | D.①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在容积为1 L的密闭容器中,加入5 mol A物质,在一定条件下同时发生下列两个反应:①2A(g)  2B(g)+C(g);②A(g)
2B(g)+C(g);②A(g)  C(g)+D(g).当达到平衡时,测得c(A)= 2.5 mol/L,c(C)=2.0 mol/L.则下列说法中正确的是
C(g)+D(g).当达到平衡时,测得c(A)= 2.5 mol/L,c(C)=2.0 mol/L.则下列说法中正确的是
A.达到平衡时A的总转化率为40%
B.达到平衡时c(B)为1.0 mol/L
C.达到平衡时c(B)=2c(D)
D.达到平衡时c(D)=2c(B)
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
硫酸是一种重要的化工产品,硫酸的消耗量常被视为一个国家工业发达水平的一种标志。目前主要生产方法是“接触法”,有关2SO2+O2 2SO3的说法中,不正确的是
2SO3的说法中,不正确的是
| A.该反应为可逆反应,故在一定条件下SO2和O2不可能全部转化为SO3 |
| B.达到平衡后,反应就停止了,故正、逆反应速率相等且均为零 |
| C.一定条件下,向某密闭容器中加入2 mol SO2和1 mol O2,则从反应开始到达到平衡的过程中,正反应速率不断减小,逆反应速率不断增大,某一时刻之后,正、逆反应速率相等 |
| D.平衡时SO2、O2、SO3的分子数之比不再改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
对于100mL 1mol/L盐酸与锌粒的反应,采取下列措施能使放出H2速率加快的是
①升高温度
②改用100mL 1mol/L硫酸
③多用300mL 1mol/L盐酸;
④用等量锌粉代替锌粒
⑤改用100mL 6mol/L硝酸
⑥滴入几滴硫酸铜溶液
⑦用粗锌代替纯锌使用
| A.①③④⑤⑦ | B.①②④⑥⑦ | C.②③④⑤⑥ | D.①②③⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
密闭容器中,反应xA(g)+yB(g)  zC(g)达平衡时,A的浓度为0.5mol/L,若保持温度不变,将容器的容积扩大到原来的2倍,达新平衡时A的浓度降为0.3mol/L下列判断错误的是 ( )
zC(g)达平衡时,A的浓度为0.5mol/L,若保持温度不变,将容器的容积扩大到原来的2倍,达新平衡时A的浓度降为0.3mol/L下列判断错误的是 ( )
| A.x+y>z | B.平衡向正方向移动 |
| C.B的转化率降低 | D.C的体积分数下降 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
一定温度下,可逆反应H2(g)+I2(g) 2HI(g)达到化学平衡状态的标志是( )
2HI(g)达到化学平衡状态的标志是( )
| A.混合气体的压强不再变化 | B.混合气体的颜色不再变化 |
| C.反应速率v(H2)="0.5v" (HI) | D.c (H2):c(I2):c(HI)=1:1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(7分)CO可用于合成甲醇,一定温度下,向体积为2L的密闭容器中加入CO和H2,发生反应CO(g)+2H2(g) CH3OH(g),达平衡后测得各组分浓度如下:
CH3OH(g),达平衡后测得各组分浓度如下:
| 物质 | CO | H2 | CH3OH |
| 浓度(mol?L-1) | 0.9 | 1.0 | 0.6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com