
硫酸钾和硫酸铝的混合溶液,已知其中Al3+的浓度为0.4 mol/L,硫酸根离子浓度为0.7 mol/L,则K+的物质的量浓度为
A.0.1 mol/L B.0.15 mol/L
C.0.3 mol/L D.0.2 mol/L
科目:高中化学 来源:2014秋贵州省遵义市高二上学期期中化学(文)试卷(解析版) 题型:选择题
欲将蛋白质从水中析出而又不改变它的性质,应加入
A.(NH4)2SO4溶液 B.酒精溶液
C.Pb(NO3)2溶液 D.NaOH溶液
查看答案和解析>>
科目:高中化学 来源:2014秋福建省高二上学期期中化学(文)试卷(解析版) 题型:选择题
工业生产和日常生活中,如何减少二氧化碳排放已成为全世界关注的热点,低碳经济和低碳生活成为热门话题。以下做法与低碳要求不相适应的是
A.尽量不使用一次性竹、木筷子
B.多挖煤,多发电,加快经济发展
C.利用特殊材料建屋顶、墙面,充分利用太阳光照明
D.提倡骑自行车、乘公交车出行
查看答案和解析>>
科目:高中化学 来源:2014秋湖北省武汉市高二上学期期中联考化学试卷(解析版) 题型:选择题
已知:断裂下列化学键需要吸收的能量分别为:H-H 436 kJ/mol;F—F 153 kJ/mol;H—F 565 kJ/mol。下列说法正确的是
A.H2与F2反应的热化学方程式为:H2(g) + F2(g)= 2HF(g); △H = -541 kJ
B.2 L HF气体分解成1 L H2和1 L F2吸收541 kJ的热量
C.在相同条件下,1 mol H2与1 mol F2的能量总和大于2 mol HF气体的能量
D.1 mol H2与1 mol F2反应生成2 mol液态HF放出热量小于541 kJ
查看答案和解析>>
科目:高中化学 来源:2014秋湖北省武汉市高一上学期期中联考化学试卷(解析版) 题型:填空题
(14分)铜既能与稀硝酸反应,也能与浓硝酸反应,当铜与一定浓度硝酸反应时,可将方程式表示为:Cu+HNO3→Cu(NO3)2+NO↑+NO2↑+H2O (方程式未配平)
(1)硝酸在该反应中表现出的性质是_____,该反应的还原产物是_____。
(2)0.4molCu被硝酸完全溶解后,硝酸得到的电子数是_____,如果得到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量是_____mol。
(3)0.3molCu被另一浓度的硝酸完全溶解后,如果此时产生的NO和NO2气体总体积在标准状况下为8.96 L,则被还原的硝酸的物质的量是_____ mol,参加反应的硝酸的物质的量是_____mol,产生的混合气体中NO和NO2体积比为_______。
查看答案和解析>>
科目:高中化学 来源:2014秋湖北省武汉市高一上学期期中联考化学试卷(解析版) 题型:选择题
在强酸性溶液中能大量共存的离子组是
A.K+、Na+、NO3-、CO32-
B.K+、Na+、Br-、SO32-
C.K+、Na+、I-、SO42-
D.Na+、K+、CH3COO-、SO42-
查看答案和解析>>
科目:高中化学 来源:2014秋湖北省武汉市高一上学期期中联考化学试卷(解析版) 题型:选择题
现有三组实验:①除去混在植物油中的水 ②将海水制成淡水 ③用食用酒精浸泡中草药提取其中的有效成份。上述分离方法依次是
A.分液、萃取、蒸馏 B.萃取、蒸馏、分液
C.分液、蒸馏、萃取 D.蒸馏、萃取、分液
查看答案和解析>>
科目:高中化学 来源:2014秋浙江省杭州地区六校高二上学期期中考试化学试卷(解析版) 题型:选择题
对于下列各组反应,反应开始时,产生氢气速率最快的是
A.70℃,将0.1 mol 镁粉加入到10 mL 6 mol·L-1 的硝酸溶液中
B.60℃,将0.2 mol 镁粉加入到20 mL 3 mol·L-1 的盐酸溶液中
C.60℃,将0.1 mol 镁粉加入到10 mL 3 mol·L-1 的硫酸溶液中
D.60℃,将0.2 mol 铁粉加入到10 mL 3 mol·L-1 的盐酸溶液中
查看答案和解析>>
科目:高中化学 来源:2014秋河北省、临漳一中、永年二中高二上学期期中联考化学试卷(解析版) 题型:填空题
(14分)如图所示,甲、乙两装置电极材料都是铁棒与碳棒,请回答下列问题:
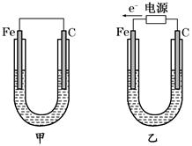
(1)若两装置中均为CuSO4溶液,反应一段时间后:
①有红色物质析出的是甲装置中的________棒,乙装置中的________棒。
②乙装置中阳极的电极反应式是:_______________________________。
(2)若两装置中均为饱和NaCl溶液:
①写出乙装置中总反应的离子方程式:_____________________________。
②甲装置中碳极的电极反应式是 ,乙装置碳极的电极反应属于________(填“氧化反应”或“还原反应”)。
③将湿润的淀粉KI试纸放在乙装置碳极附近,发现试纸变蓝,解释其原因: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com