
 向某碳酸钠溶液中逐滴加1mol?L-1的盐酸,侧得溶液中Cl-、HCO3-的物质随加入盐酸体积的关系如图所示,则下列说法中正确的是( )
向某碳酸钠溶液中逐滴加1mol?L-1的盐酸,侧得溶液中Cl-、HCO3-的物质随加入盐酸体积的关系如图所示,则下列说法中正确的是( )| A、b点的数值为0.6 |
| B、该碳酸钠溶液中含有1molNa2CO3 |
| C、Oa段反应的离子方程式与ab段反应的离子方程式相同 |
| D、a点时加入的盐酸为0.5mol,此时生成CO2的物质的量为0.25mol |


科目:高中化学 来源: 题型:
| A、溶解CuSO4?5H2O晶体时要加入少量稀H2SO4 |
| B、加入H2O2,除Fe2+的离子方程式:2Fe2++H2O2+4OH-═2 Fe(OH)3 |
| C、由于CuSO4的催化作用,会使部分H2O2分解而损失 |
| D、调溶液pH=4的依据是当pH=4时Fe(OH)3沉淀完全,而Cu(OH)2还未开始沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、①② | B、②③ | C、③④ | D、①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、所得溶液中的c (H+)=10-13 mol.L-1 |
| B、所得溶液中由水电离产生的c(OH -)=10-13mol.L-1 |
| C、所得溶液中的c (Mg2+)=5.6×l0-10 mol.L-1 |
| D、所加烧碱溶液的pH=13.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 利用碳纳米管能吸附氢气,设计一种新型二次电池,其装置如图所示,关于该电池的叙述不正确的是( )
利用碳纳米管能吸附氢气,设计一种新型二次电池,其装置如图所示,关于该电池的叙述不正确的是( )| A、电池放电时K+移向正极 |
| B、电池放电时负极反应为:H2-2e-+2OH-═2H2O |
| C、电池充电时镍电极NiOOH转化为Ni(OH)2 |
| D、电池充电时碳纳米管电机与电源的负极相连. |
查看答案和解析>>
科目:高中化学 来源: 题型:
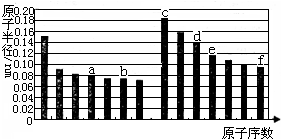
| A、a的单质在高温条件下能置换出e的单质,说明非金属性a<e |
| B、b、d两种元素的离子半径相比,前者较大 |
| C、由b、e两种元素组成的化合物能溶解于强碱溶液,但不能与酸溶液反应 |
| D、由c、d分别与f组成的化合物中的化学键类型相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、次氯酸的结构式:H-Cl-O |
B、O2的电子式: |
| C、葡萄糖的实验式:CH2O |
| D、能说明碳酸钙为强电解质的表达式:CaCO3(s)?Ca2+(aq)+CO32-(aq) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com