
| A、钠 | B、铁 | C、镁 | D、铜 |
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:高中化学 来源: 题型:
| A、CaSO4 |
| B、CaCl2 |
| C、CaCO3 |
| D、Ca(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径:C>D>A>B |
| B、原子序数:C>D>B>A |
| C、离子半径:D>C>B>A |
| D、单质的还原性:B>A>C>D |
查看答案和解析>>
科目:高中化学 来源: 题型:
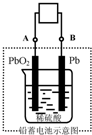 如图所示,铅蓄电池是一种典型的可充电电池,电池总反应式为:Pb+PbO2+4H++2SO42-
如图所示,铅蓄电池是一种典型的可充电电池,电池总反应式为:Pb+PbO2+4H++2SO42-| 放电 |
| 充电 |
| A、放电时,正极反应是Pb-2e-+SO42-=PbSO4 |
| B、放电时,外电路中电子流动方向由B到A |
| C、放电时,铅蓄电池的负极质量增加,正极质量减小 |
| D、充电时,该装置中化学能转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AgNO3 |
| B、CuSO4 |
| C、MgSO4 |
| D、Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③⑤⑥ | B、②③⑤⑥ |
| C、①②④ | D、②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、②③ | C、①③ | D、①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:

浓度/mol?L-1 时间/min |
NO | N2 | CO2 |
| 0 | 0.100 | 0 | 0 |
| 10 | 0.058 | 0.021 | 0.021 |
| 20 | 0.040 | 0.030 | 0.030 |
| 30 | 0.040 | 0.030 | 0.030 |
| 40 | 0.032 | 0.034 | 0.017 |
| 50 | 0.032 | 0.034 | 0.017 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com