
����Ŀ��ij�о���ѧϰС�����ⶨ�����£�25�桢101kPa��������Ħ���������ش��������⣮��С����Ƶļ���ʵ��װ����ͼ��ʾ�� 
��ʵ�����Ҫ�����������£�
������100mL 1.0molL��1��������Һ��
���á���������.�����������Ʋ�ע�������ȡ7.5mL 1.0molL��1��������Һ������ƿ�У�
�۳�ȡa g�ѳ�ȥ��������Ĥ��þ������ϵ��ͭ˿ĩ�ˣ�ΪʹHClȫ���μӷ�Ӧ��a����ֵ����Ϊ����������.g��
�������ƿ��װ������ˮ������ͼ���Ӻ�װ�ã����װ�õ������ԣ�
�ݷ�Ӧ���������ϵ�¶Ȼָ������£�������Ͳ��ˮ�����ΪV mL��
�뽫�������貹���������ش��������⣮
��1��������У�����100mL 1.0molL��1��������Һʱ��������Щ������ʹ����Ũ��ƫС�� ������д��ĸ����
A.����Ͳ��ȡŨ����ʱ��������Ͳ�Ŀ̶�
B.����ƿδ���T����������Һ
C.Ũ�������ձ���ϡ��ʱ������ʱ�����
D.������ɺ�����ƿ����ҡ�Ⱥ���Һ����ڿ̶���
E.������ƿ�ж���ʱ��������ƿ�̶���
F.�ձ���������ˮ
��2������д���������еĿո���� �� �����g��
��3��ʵ�鲽�����Ӧѡ���� ��������ĸ������Ͳ��
A.100mL
B.200mL
C.500mL
��4������ˮ����Ӱ�죬�ڸ������²������Ħ������ļ���ʽΪVm=L/mol��
��5����δ��ȥþ�����������Ĥ�����ø������������Ħ���������ƫ��ƫС����Ӱ�죩��
���𰸡�
��1��AC
��2��10mL��Ͳ��0.09
��3��A
��4��![]()
��5��ƫ��
���������⣺��1��A������Ͳ��ȡŨ����ʱ��������Ͳ�Ŀ̶ȣ�����ȡ��Ũ��������ƫС�������ó�����Һ��Ũ��ƫ�ͣ���A��ȷ��
B������ƿδ���T����������Һ������Һ��Ũ����Ӱ�죬��B����
C��Ũ�������ձ���ϡ��ʱ������ʱ������ᵼ��HCl�Ļӷ����������õ���Һ��Ũ��ƫ�ͣ���C��ȷ��
D��������ɺ�����ƿ����ҡ�Ⱥ���Һ����ڿ̶����������ģ���D����
E��������ƿ�ж���ʱ��������ƿ�̶��ߣ�����Һ���ƫС��Ũ��ƫ�ߣ���F����
F���ձ���������ˮ�����������ʵ�����Ӱ�죬��������Ƶ���Һ��Ũ����Ӱ�죬��F����
��ѡAC����2���������ȡ7.5mL 1.0molL��������Һ������ƿ�У�����Ҫ��������7.5mL����ѡ��10mL��Ͳ���ɣ�
�����
Mg+ | 2HCl�TMgCl2+H2�� |
1mol | 2mol |
n | 0.0075 mol |
n=0.00375mol ��a=24g/mol��0.00375mol=0.090��
�ʴ�Ϊ��10mL��Ͳ��0.09g����3��
Mg+ | 2HCl�TMgCl2+ | H2�� |
2mol | 1mol | |
0��0075 mol | n��H2�� |
n��H2��=0.00375mol
V��H2��=0.00375 mol��22.4L/mol=0.084L=84ml��Ӧѡ100mL��Ͳ��
�ʴ�Ϊ��A����4���ɣ�2������������ʵ���Ϊ0.00375 mol��ͨ������������ΪV mL��Vm= ![]() =
= ![]() =
= ![]() L/mol��
L/mol��
�ʴ�Ϊ�� ![]() ����5����δ��ȥþ�����������Ĥ�����ɵ�����������٣���������ƫ�ͣ��ʴ�Ϊ��ƫ�ͣ�
����5����δ��ȥþ�����������Ĥ�����ɵ�����������٣���������ƫ�ͣ��ʴ�Ϊ��ƫ�ͣ�
��1���������������n��V��Ӱ�죬����c= ![]() ����������������ҺŨ�ȵ�Ӱ�죮��2���������ȡ7.5mL 1.0molL��������Һ������ƿ�У�����Ҫ��������7.5mL����ѡ��10mL��Ͳ���ɣ�
����������������ҺŨ�ȵ�Ӱ�죮��2���������ȡ7.5mL 1.0molL��������Һ������ƿ�У�����Ҫ��������7.5mL����ѡ��10mL��Ͳ���ɣ�
����ۼ���aȫ����þ��ϻ�ѧ����ʽ����õ�����3��Mg+2HCl�TMgCl2+H2�������������������Ϊ�ų���ˮ��������ݴ�ѡ����Ͳ�Ĺ��4���ɣ�3������������ʵ���Ϊ0.00375mol��ͨ����������ΪV mL��ͨ��Vm= ![]() �����㣻��5����δ��ȥþ�����������Ĥ�����ɵ�����������٣�
�����㣻��5����δ��ȥþ�����������Ĥ�����ɵ�����������٣�


 һ����ʦ�����Ծ�ϵ�д�
һ����ʦ�����Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����г�ȥ������ѡ�õ��Լ���ȷ���ǣ� ��
A. ��ȥN2 �л��е�O2��ѡ�����ȵ�ͭ��
B. ��ȥCO2�л��е�CO��ѡ�ó���ʯ��ˮ
C. ��ȥBaCO3�����л��е�BaSO4��ѡ��ϡ����
D. ��ȥFe���л��е�Cu �ۣ�ѡ��ϡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A�뷼���廯����B��һ�������·�Ӧ����C����һ����Ӧ�����л���D��D�Ķ�ˮ������ҽѧ�ϳ�֮Ϊ�����أ���һ������ƫͷʹ����Ч��ҩ��A����Է���������104��1mol A��������NaHCO3��Ӧ����2mol���壮 ��֪��RCHO+CH2��COOH��2 ![]() RCH=C��COOH��2+H2O��
RCH=C��COOH��2+H2O��
RCH=C��COOH��2 ![]() RCH=CHCOOH+CO2
RCH=CHCOOH+CO2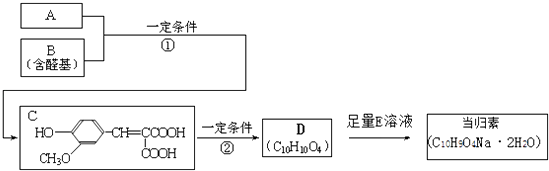
��1��C���ܷ����ķ�Ӧ��������ţ��� a��������Ӧ b��ˮ�ⷴӦ c����ȥ��Ӧ d��������Ӧ
��2�������ʵ�����C�ֱ���������Na��NaHCO3��NaOH��Ӧ����Na��NaHCO3��NaOH�����ʵ���֮���� ��
��3��E�����ƣ� ��
��4����Ӧ�ٵĻ�ѧ����ʽ�� ��
��5����������������D��ͬ���칹�����֣�д����������һ�ֵĽṹ��ʽ �� ���ڱ�����ֻ������ȡ���������ڱ����ϵ�һ��ȡ����ֻ�����֣�
��1mol��ͬ���칹����������NaHCO3��Ӧ��2mol CO2 ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����mgþ�����Ļ�����ؼ���������ϡ���ᣬǡ����ȫ��Ӧ���ɱ�״���µ�����bL����Ӧ�����Һ�м���cmol/L����������ҺVmL��ʹ�������Ӹպó�����ȫ���õ��ij�������Ϊng���ٽ��õ��ij����������������ٸı�Ϊֹ���õ�����pg�������й�ϵ����ȷ���ǣ�������
A.c= ![]()
B.p=m+ ![]()
C.n=m+17Vc
D.![]() m��p��
m��p�� ![]() m
m
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ᱽ��������������������������㾫�ĵ������ϣ��������üױ����Ҵ�Ϊԭ�Ͻ����˹��ϳɣ��ϳ�·�����£� 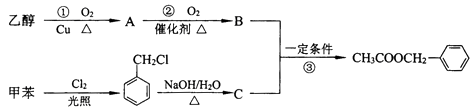
��1��C�Ľṹ��ʽΪ ��
��2����Ӧ�ڡ��۵ķ�Ӧ����Ϊ �� ��
��3���ױ���һ�ȴ������֣�
��4��д����Ӧ�ٵĻ�ѧ����ʽ ��
��5��Ϊ��������ᱽ�����IJ���Ӧ��ȡ�Ĵ�ʩ�ǣ�дһ� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ƴ���Ư����ɱ���������������������Ʊ��治���������տ�����CO2�����ʣ�
��1��ij����С����̽��ij����������Ʒ�Ƿ��Ѿ����ʣ�ȡ������Ʒ���ܽ⣬������Һ��������а�ɫ������֤��Na2O2�Ѿ����ʣ�
��2���ÿ���С��Ϊ�˴��Բⶨ�������ƵĴ��ȣ����dz�ȡa g��Ʒ�����������ͼװ�����ⶨ�������Ƶ����������� 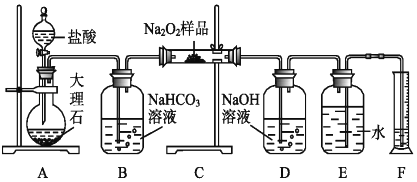
��A�з�����Ӧ���ӷ���ʽΪ ��
�ڽ��������Ӻ��Ժ�����еĵ�һ�������� ��
��Bװ�ó����������Ƿ���Ҫ���� �� ����ǡ���
��д��װ��C�з��������з�Ӧ�Ļ�ѧ����ʽ �� ��
��D��NaOH��Һ������ ��
��ʵ�����ʱ����ȡʵ����������������ʱ������������ ��
a��ֱ�Ӷ�ȡ���������������ȴ������
b�������ƶ���Ͳ��ʹ��E��F��Һ��߶���ͬ
c�������밼Һ�����͵���ƽ��ȡ��Ͳ��ˮ�����
�߶�����Ͳ��ˮ�����������ɱ�״�������������ΪV mL������Ʒ�й������Ƶ���������Ϊ ��
��ʵ����ɺ�E��F֮�䵼���ڲ���ˮ�������ʹ������� �� ���ƫ����ƫС����Ӱ�족��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼����������������ǶԴ�����ò�ͬ���෨�ķ��࣬������ȷ����( )
(1)�� (2)�������� ��3������ ��4��̼����
A. (1)(2)(3) B. (1)(3)(4) C. (1)(2)(4) D. (2)(3)(4)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ù���KOH����0.1mol/L��KOH��Һ480mL���ش��������⣺
��1�����ƹ�������Ҫ�õ��IJ����������ձ�������������Ͳ����ͷ�ιܡ�
��2����Ҫ��������ƽ����gKOH���壮
��3������ڶ���ʱ���Ӳ��������������Һ��Ũ��0.1mol/L �����=������
��4�������õĹ���KOH�л���NaOH�����������Һ��c��OH����Ũ��0.1mol/L �����=������
��5��II�����ڷ�����ᴿ���ʵķ����У�A��������B����ȡ��C�����ˣ�D����Һ��E�����������и�������ķ�����ᴿӦѡ��������һ�ַ�������ʣ�������ı�ţ� �ٷ������Ȼ�̼��ˮ�Ļ������
�ڷ�����ۺ�NaCl��Һ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com