
| A. | 在水溶液和熔融状态下能导电的化合物,叫做电解质 | |
| B. | 在水溶液或熔融状态下能导电的化合物,叫做电解质 | |
| C. | BaSO4是难溶物,所以是非电解质 | |
| D. | 氧化还原反应的本质是化合价升降 |
分析 A.在水溶液里或熔融状态下能导电的化合物为电解质,是“或”,不是“和”;
B.电解质是在水溶液或者熔融状态下能导电的化合物;
C.硫酸钡是难溶的盐,熔融状态完全电离;
D.氧化还原反应的特征是元素化合价的升降,实质是电子的转移.
解答 解:A.电解质必须满足在水溶液里或熔融状态下能导电的化合物,在水溶液里、熔融状态下两者只需具备其一即可,不是都需具备,如氯化氢为电解质,属于只有在水溶液状态下能导电的化合物,故A错误;
B.电解质定义为在水溶液中或熔融状态下能导电的化合物,故B正确;
C.硫酸钡是难溶的盐,熔融状态完全电离;所以BaSO4是电解质,故C错误;
D.氧化还原反应的本质是电子的转移,故D错误.
故选B.
点评 本题考查了电解质的概念、氧化还原反应本质,注重了基础知识的考查,题目难度不大,注意掌握电解质与非电解质的概念与区别,明确电解质的概念中用“或”的含义.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | B的阳离子的氧化性比A的阳离子强,说明A元素的金属性一定比B元素强 | |
| B. | 在氧化还原反应中,肯定有一种元素被氧化,另一种元素被还原 | |
| C. | 一种元素可能有多种氧化物,但同一化合价只对应一种氧化物 | |
| D. | 强氧化剂与强还原剂不一定能发生氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有0.1mol•L-1Fe3+的溶液中:K+、Mg2+、I-、NO3- | |
| B. | 室温下,pH=1的溶液中:Na+、Fe3+、NO3-、SO42- | |
| C. | 加入铝粉有气泡产生的溶液中:Na+、NH4+、Fe2+、NO3- | |
| D. | 在AlCl3溶液中:K+、Na+、SiO32-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2L四氯化碳所含分子数为0.5NA | |
| B. | 1L1mol/l的盐酸溶液中,所含氯化氢分子数为NA | |
| C. | 标准状况下,0.5molCO2所占的体积约为11.2L | |
| D. | 11.2L氧气所含的原子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
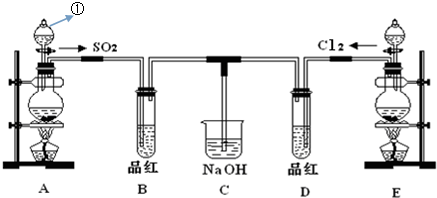
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使pH试纸呈红色的溶液中:Na+、AlO2-、NO3-、CO32- | |
| B. | 遇苯酚溶液显紫色的溶液:Na+、SO32-、S2-、Cl- | |
| C. | 含有0.1 mol•L-1 HCO3-的溶液:Na+、K+、NO3-、C6H5O- | |
| D. | 水电离出的H+浓度为1.0×10-12 mol•L-1的溶液:Na+、Fe3+、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 nm左右 | B. | 50 nm左右 | C. | 0.001 mm左右 | D. | 100 mm左右 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中子数为20的氯原子:1720Cl | B. | S2-的结构示意图: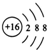 | ||
| C. | 四氯化碳的电子式: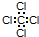 | D. | 乙醇的结构式:C2H6O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com