
【题目】用已知浓度的盐酸滴定未知浓度的NaOH溶液时,下列操作中不正确的是
A.酸式滴定管用蒸馏水洗净后,必须用已知浓度的盐酸润洗
B.锥形瓶用蒸馏水洗净后,用NaOH溶液润洗后再加入待测液
C.滴定时,必须逐出滴定管下口的气泡
D.读数时,视线与滴定管内液体的凹液面最低处保持水平
 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:
【题目】用 NA 表示阿伏加德罗常数的值,下列叙述中正确的是
A. 常温常压下,17g 甲基(-14CH3)所含的中子数为 9 NA
B. 电解精炼铜的过程中,若阳极减轻 64 g,则电路中一定通过 2NA 个电子
C. NA 个 Fe(OH)3 胶体粒子的质量为 107 g
D. 1mol 铜与足量硫蒸气反应,转移电子数为 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】血液中的葡萄糖称为血糖,空腹血糖是筛査糖尿病的常用指标,正常范围在3.9-6.1mmol/L(注:1m mol/L= 1×10-3 mol/L);该体检指标表示的是
A.物质的量(n)B.物质的量浓度(c)C.质量分数(ω)D.摩尔质量(M)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于pH变化的判断正确的是( )
A.温度升高,Na2CO3溶液pH减小B.温度升高,纯水pH增大
C.新制氯水经光照一段时间后,溶液pH减小D.氢氧化钠溶液久置于空气中,溶液pH变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示。请回答:

(1)若C为稀H2SO4溶液,电流表指针发生偏转,B电极材料为Zn,A极材料为铜,该装置能量转换形式____, A为____极,此电池所发生的反应化学方程式为_____,反应进行一段时间后溶液C中c(H+)将_____(填“变大” “变小”或“基本不变”)。溶液中的SO42-移向____极(填“A”或“B”)
(2)若C为CuSO4溶液,B电极材料为Fe,A极材料为石墨。则B为_____极,B极上电极反应属于____(填“氧化反应”或“还原反应”)。B电极上发生的电极反应式为______,A极产生的现象是_____;若AB两电极质量都为50.0g且反应过程中有0.2mol的电子发生转移,理论上AB两电极质量差为____g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四氯化钛(TiCl4)是制取航天航空工业材料——钛合金的重要原料。由钛铁矿(主要成分是FeTiO3)制备TiCl4,同时获得副产品甲的工业生产流程如下:
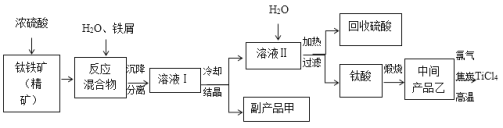
(1)已知酸浸反应FeTiO3+2H2SO4===FeSO4+TiOSO4+2H2O,则FeTiO3中铁元素的化合价为___________。
(2)上述生产流程中加入铁屑的目的是使Fe3+还原为Fe2+,且反应得到的溶液中含钛元素的离子只有TiO2+,该过程发生的主要反应有:
①2Fe3++Fe===3Fe2+ ; ②2TiO2++Fe+4H+===2Ti3++Fe2++2H2O;③______________________________________。
(3)加热TiOSO4溶液可制备TiO2·nH2O胶体,其反应的化学方程式为__________________。
(4)由TiO2·nH2O胶体制得固体TiO2·nH2O,再用酸清洗除去其中的Fe(OH)3杂质,还可制得钛白粉。已知25℃时,Ksp[Fe(OH)3]=2.79×10-39,该温度下反应Fe(OH)3+3H+![]() Fe3++3H2O的平衡常数K=___________________。
Fe3++3H2O的平衡常数K=___________________。
(5)可循环利用的物质是_________,副产品甲含结晶水,其化学式是_______________。
(6)依据下表信息,要精制含少量SiCl4杂质的TiCl4,可采用___________方法。
TiCl4 | SiCl4 | |
熔点/℃ | -25.0 | -68.8 |
沸点/℃ | 136.4 | 57.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是CO和水蒸气发生反应生成CO2和H2的途径和三个状态的能量,该反应为吸热反应,试问:
E1:CO+H2O![]() E2:C+2H+2O
E2:C+2H+2O![]() E3:CO2+H2
E3:CO2+H2
(1)步骤1、2分别是吸热过程还是放热过程?
步骤1:______,步骤2:______。
(2)比较E1、E3的大小______。
(3)已知,25℃时,C(石墨)+1/2O2(g) ═ CO(g) ΔH1=-111 kJ/mol;
H2(g)+1/2O2(g) ═ H2O(g) ΔH2=-242 kJ/mol;
C(石墨)+O2(g) ═ CO2(g) ΔH3=-394 kJ/mol。
则CO和H2O(g)反应的热化学方程式为:______。
(4)含1 mol Ba(OH)2的稀溶液与足量稀盐酸反应放出114.6 kJ的热量,写出该反应中和热的热化学方程式:______。
(5)在C2H2(g)完全燃烧生成CO2和液态水的反应中,每转移5NA个电子放出a kJ的热量。则表示C2H2的燃烧热的热化学方程式为:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO(g)与H2O(g)反应的能量变化如图所示,有关两者反应的说法正确的是( )

A. 该反应为吸热反应
B. 该反应不需要加热就能进行
C. 1 molCO(g)和1mol H2O(g)具有的总能量大于1 molCO2(g)和1 molH2(g)具有的总能量
D. 1 molCO2(g)和1 molH2(g)反应生成1 molCO(g)和1mol H2O(g)要放出41 kJ热量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com