
| A. | 大于10种 | B. | 10种 | C. | 6种 | D. | 5种 |
分析 芳香族化合物的分子式为C8H10O,故A含有1个苯环,遇三氯化铁溶液不显色,不含有酚羟基,能与金属钠反应放出氢气,则含醇羟基,侧链可能是-CH2CH2OH或-CHOHCH3或有-CH2OH和-CH3,-CH2OH和-CH3有邻、间、对三种位置异构,据此解答.
解答 解:芳香族化合物的分子式为C8H10O,故A含有1个苯环,遇三氯化铁溶液不显色,不含有酚羟基,能与金属钠反应放出氢气,则含醇羟基,侧链可能是-CH2CH2OH或-CHOHCH3或有-CH2OH和-CH3,-CH2OH和-CH3有邻、间、对三种位置异构,共有5种同分异构体,故选D.
点评 本题考查同分异构体、有机物结构的推断、官能团的性质等,难度不大,确定苯环含有的侧链是关键.


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:解答题
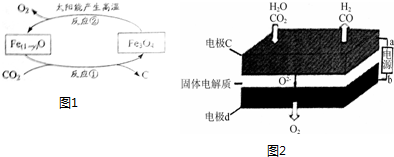
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | PCl5 分子中所有原子都满足最外层8电子稳定结构且共用电子对发生偏移 | |
| B. | 两个原子间形成共价键时,最多可以有两个σ键 | |
| C. | H3O+中H-O-H的键角比H2O中H-O-H的键角大 | |
| D. | 酸性强弱比较:HClO>HClO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧的五种同位素 | B. | 五种氧元素 | ||
| C. | 氧的五种同素异形体 | D. | 氧元素的五种不同微粒 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
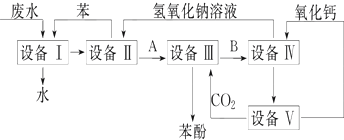
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O2是还原剂,PtF6是氧化剂 | |
| B. | O2(PtF6)中氧元素的化合价为-2 | |
| C. | O2(PtF6)中不存在共价键 | |
| D. | 每生成1mol O2(PtF6)则转移2mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 水的电离平衡曲线如图所示:
水的电离平衡曲线如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com