
 ŅŃÖŖSO2+I2+2H2OØTH2SO4+2HI£¬Ä³»ÆѧŠĖȤŠ”×éŃ”ÓĆĻĀĮŠŹµŃé×°ÖĆ£¬²ā¶Ø¹¤ŅµŌĮĻĘų£Øŗ¬SO2”¢N2”¢O2£©ÖŠµÄSO2µÄŗ¬Į森
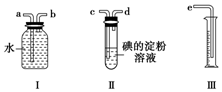
ŅŃÖŖSO2+I2+2H2OØTH2SO4+2HI£¬Ä³»ÆѧŠĖȤŠ”×éŃ”ÓĆĻĀĮŠŹµŃé×°ÖĆ£¬²ā¶Ø¹¤ŅµŌĮĻĘų£Øŗ¬SO2”¢N2”¢O2£©ÖŠµÄSO2µÄŗ¬Į森·ÖĪö £Ø1£©ŌĮĻĘųĶعżµāµÄµķ·ŪČÜŅŗ£¬µāÄÜŃõ»ÆH2SO3£¬Éś³ÉH2SO4 £¬ĪüŹÕ¶žŃõ»ÆĮņĘųĢ壬Ķعż×°ÖĆ¢ń¢óÅÅĖ®ĮæĘų²ā¶ØŅĒĘ÷ŗĶµŖĘųµÄĢå»ż£»
£Ø2£©×°ÖĆ¢ņŹĒĪüŹÕ¶žŃõ»ÆĮņĘųĢ壬µāµÄµķ·ŪČÜŅŗŹĒĄ¶É«£¬µ±Ą¶É«ĶŹČ„£¬ĖµĆ÷µāµ„ÖŹČ«²æ·“Ó¦£¬Ó¦Ķ£Ö¹ĶØĘų£»
£Ø3£©ŅĄ¾Żµāµ„ÖŹŃõ»Æ¶žŃõ»ÆĮņµÄ»Æѧ·½³ĢŹ½¼ĘĖ涞Ńõ»ÆĮņĘųĢåĢå»ż£¬µĆµ½SO2µÄĢå»ż·ÖŹż£®
½ā“š ½ā£ŗ£Ø1£©ŌĮĻĘųĶعżµāµÄµķ·ŪČÜŅŗ£¬µāÄÜŃõ»ÆH2SO3£¬Éś³ÉH2SO4 £¬ĪüŹÕ¶žŃõ»ÆĮņĘųĢ壬Ķعż×°ÖĆ¢ń¢óÅÅĖ®ĮæĘų²ā¶ØŅĒĘ÷ŗĶµŖĘųµÄĢå»ż£¬Į¬½Ó×°ÖĆ½ÓæŚĖ³ŠņĪŖ£ŗc”śd”śb”śa”śe£»
¹Ź“š°øĪŖ£ŗc”śd”śb”śa”śe£»
£Ø2£©×°ÖĆ¢ņŹĒĪüŹÕ¶žŃõ»ÆĮņĘųĢ壬µāµÄµķ·ŪČÜŅŗŹĒĄ¶É«£¬µ±Ą¶É«ĶŹČ„£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗĖµĆ÷µāµ„ÖŹČ«²æ·“Ó¦£¬Ó¦Ķ£Ö¹ĶØĘų£¬·ńŌņ¶žŃõ»ÆĮņĪüŹÕ²»ĶźČ«£¬Ōģ³ÉĪó²ī£»
¹Ź“š°øĪŖ£ŗĄ¶É«Ē”ŗƱä³ÉĪŽÉ«£»
¹Ź“š°øĪŖ£ŗSO2+I2+2H2OØT4H++SO42-+2I-£»Ą¶É«ĶŹČ„£»
£Ø3£©·“Ó¦·½³ĢŹ½I2+SO2+2H2O=2I-+SO42-+4H+
ÓÉĢõ¼žÖŖn£ØSO2£©=n£ØI2£©=0.05 mol/L”Į0.02 L=0.001 mol£¬¼“22.4 mL£¬
ĖłŅŌ¹¤ŅµŌĮĻĘų×ÜĢå»żĪŖ 297.6 mL+22.4 mL=320 mL£¬
SO2µÄĢå»ż·ÖŹż=$\frac{22.4ml}{320ml}$”Į100%=7%£¬
¹Ź“š°øĪŖ£ŗ7%£®
µćĘĄ ±¾Ģāæ¼²éĮĖ¶žŃõ»ÆĮņŠŌÖŹ·ÖĪö£¬“¦Ąķ·½·ØŗĶ¼ĘĖćÓ¦ÓĆ£¬×¢ŅāŹµŃé²ā¶Ø¹ż³ĢµÄ·ÖĪöÅŠ¶Ļ£¬ÕĘĪÕ»ł“”ŹĒ¹Ų¼ü£¬ĢāÄæÄѶČÖŠµČ£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1L 1mol/LµÄHClČÜŅŗÖŠĖłŗ¬ĀČ»ÆĒā·Ö×ÓŹżĪŖNA | |
| B£® | Ģå»żĪŖ6L µÄ O2£¬ĘäÖŹĮæ²»æÉÄÜĪŖ8 g | |
| C£® | 1 mol FeCl3ĶźČ«×Ŗ»ÆĪŖFe£ØOH£©3½ŗĢåŗóÉś³ÉNAøö½ŗĢåĮ£×Ó | |
| D£® | 1mol ¹żŃõ»ÆÄĘÖŠŅõĄė×ÓĖł“ųµēŗÉŹżĪŖ2NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Č”Ņ»¶ØĮæ¹ĢĢ壬Čܽā£¬ĻņČÜŅŗÖŠ¼ÓČėŹŹĮæCaO·ŪÄ©£¬³ä·Ö·“Ó¦ŗó¹Ū²ģµ½ÓŠ°×É«³ĮµķÉś³É£¬ĖµĆ÷Ō¹ĢĢåÖŠŅ»¶Øŗ¬ÓŠNa2CO3 | |
| B£® | Č”Ņ»¶ØĮæ¹ĢĢ壬Čܽā£¬ĻņČÜŅŗÖŠĶØČėµÄCO2£¬¹Ū²ģµ½ÓŠ¾§ĢåĪö³ö£¬ĖµĆ÷Ō¹ĢĢåÖŠŅ»¶Øŗ¬ÓŠNa2CO3 | |
| C£® | Č”Ņ»¶ØĮæ¹ĢĢ壬¼ÓČČ£¬Čō²śÉśµÄĘųĢåÄÜŹ¹³ĪĒåŹÆ»ŅĖ®±ä»ė×Ē£¬ĖµĆ÷Ō¹ĢĢåÖŠŅ»¶Øŗ¬ÓŠNaHCO3 | |
| D£® | Č”Ņ»¶ØĮæ¹ĢĢ壬µĪ¼Ó0£®l mol/LŃĪĖįÖĮ1LŹ±£¬ČÜŅŗ³ŹÖŠŠŌ£¬ĖµĆ÷¹ĢĢåÖŠø÷ĪļÖŹµÄĪļÖŹµÄĮæ×ÜŗĶĪŖ0.05 mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆÄ÷×Ó“ÓŹŌ¼ĮĘæÖŠ¼ŠČ”ÄĘæé | |
| B£® | ÓĆĖ®ĒåĻ“ŹŌ¹ÜÄŚ±Śø½×ŵÄĮņ | |
| C£® | ²ÉÓĆ”°ÉČĪÅ”±µÄ·½·ØĪÅĀČĘųµÄĘųĪ¶ | |
| D£® | ÓĆ½ą¾»µÄ²¬ĖæÕŗČ”ČÜŅŗ½ųŠŠŃęÉ«·“Ó¦µÄŹµŃé |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 0.1 mol•L-1 NH4HSČÜŅŗÖŠÓŠ£ŗc£ØNH4+£©£¼c£ØHS-£©+c£ØS2-£©+c£ØH2S£© | |
| B£® | ŌŚNaHSO4ČÜŅŗÖŠ£¬c£ØH+£©=c£ØOH-£©+c£ØSO42-£© | |
| C£® | µČÅØ¶ČµÄHCNŗĶNaCN»ģŗĻČÜŅŗÖŠÓŠ£ŗ2c£ØNa+£©=c£ØCN-£©+c£ØHCN£© | |
| D£® | µČpHµÄ¢Ł£ØNH4£©2SO4ČÜŅŗ””¢ŚNH4HSO4ČÜŅŗ””¢ŪNH4ClČÜŅŗÖŠ£¬c£ØNH4+£©µÄ“󊔹ŲĻµ£ŗ¢Ł£¾¢Ū£¾¢Ś |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
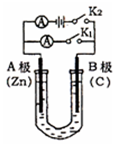 ČēĶ¼ĖłŹ¾£¬UŠĪ¹ÜÄŚŹ¢ÓŠ200mLµÄČÜŅŗ£¬°“ŅŖĒó»Ų“šĻĀĮŠĪŹĢā£®
ČēĶ¼ĖłŹ¾£¬UŠĪ¹ÜÄŚŹ¢ÓŠ200mLµÄČÜŅŗ£¬°“ŅŖĒó»Ų“šĻĀĮŠĪŹĢā£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĆŗµÄŅŗ»Æ | B£® | ŗ£Ė®É¹ŃĪ | C£® | ĄÆÖņÕÕĆ÷ | D£® | ŹÆÓĶĮŃ½ā |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·Ö×Ó¾§ĢåÖŠŅ»¶Øŗ¬ÓŠ¹²¼Ū¼ü£¬²»ŗ¬ÓŠĄė×Ó¼ü | |
| B£® | ½öŗ¬¹²¼Ū¼üµÄĪļÖŹ²»Ņ»¶ØŹĒ¹²¼Ū»ÆŗĻĪļ | |
| C£® | Ō×Ó¾§ĢåÖŠÖ»“ęŌŚ·Ē¼«ŠŌ¹²¼Ū¼ü | |
| D£® | ²»Ķ¬Ō×ÓŠĪ³ÉµÄ“æ¾»ĪļŅ»¶ØŹĒ»ÆŗĻĪļ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com