
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
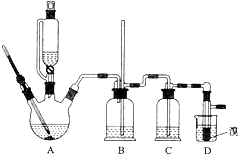
分析 (1)乙醇在浓硫酸140℃的作用下发生分子间脱水;
(2)浓硫酸具有强氧化性,可能氧化乙醇中的碳;
(3)乙烯和溴水发生了加成反应;
(4)根据1,2-二溴乙烷和水的密度相对大小解答;
(5)Br2可以和氢氧化钠发生氧化还原反应;
(6)利用1,2-二溴乙烷与乙醚的沸点不同进行解答;
(7)溴易挥发,该反应放热.
解答 解:(1)在此制各实验中,要尽可能迅速地把反应温度提高到170℃左右,因乙醇在浓硫酸140℃的条件下,发生分子内脱水,生成乙醚,
故答案为:d;
(2)浓硫酸具有强氧化性,将乙醇氧化成二氧化碳,自身被还原成二氧化硫,二氧化碳、二氧化硫均能和氢氧化钠溶液反应,则装置C中应加入NaOH溶液吸收酸性气体,
故答案为:c;
(3)乙烯和溴水发生加成反应生成1,2-二溴乙烷,1,2-二溴乙烷为无色,则判断该制备反应已经结束的最简单方法是溴的颜色完全褪去,
故答案为:溴的颜色完全褪去;
(4)1,2-二溴乙烷和水不互溶,1,2-二溴乙烷密度比水大,振荡后静置,有机产物应在下层,
故答案为:下;
(5)常温下Br2和氢氧化钠发生反应:2NaOH+Br2═NaBr+NaBrO+H2O,所以若产物中有少量未反应的Br2,最好用NaOH溶液洗涤除去,
故答案为:b;
(6)1,2-二溴乙烷与乙醚的沸点不同,两者均为有机物,互溶,用蒸馏的方法将它们分离,
故答案为:蒸馏;
(7)溴在常温下,易挥发,乙烯与溴反应时放热,溴更易挥发,则装置D中冰水冷却可避免溴的大量挥发,但1,2-二溴乙烷的凝固点9℃较低,不能过度冷却,
故答案为:乙烯与溴反应时放热,冷却可避免溴的大量挥发;1,2-二溴乙烷的凝固点较低(9℃),过度冷却会使其凝固而使气路堵塞.
点评 本题考查有机物的制备实验,为高频考点,把握有机物的结构与性质、发生的反应、实验技能为解答的关键,侧重分析与实验能力的综合考查,题目难度不大.


科目:高中化学 来源: 题型:解答题
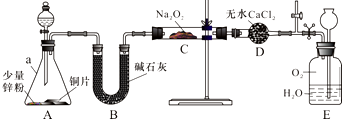 NO能否与Na2O2反应?如果能反应,产物是什么?某兴趣小组对此进行探究.
NO能否与Na2O2反应?如果能反应,产物是什么?某兴趣小组对此进行探究.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某同学利用下列实验装置图探究铜与稀硝酸反应的还原产物并进行喷泉实验(假设药品足量),请回答下列问题:
某同学利用下列实验装置图探究铜与稀硝酸反应的还原产物并进行喷泉实验(假设药品足量),请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| I1 | I2 | I3 | I4 | I5 | … | |
| R | 740 | 1500 | 7700 | 10500 | 13600 | … |
| A. | ①③ | B. | ②③ | C. | ②③④ | D. | ②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:X<Y | |
| B. | 第一电离能:X>Y | |
| C. | 气态氢化物的稳定性:HmY小于HnY | |
| D. | X与Y形成化合物时,一般显负价,Y显正价 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苹果汁中的Fe2+变成Fe3+ | B. | 苹果汁中含有Cu2+ | ||
| C. | 苹果汁含有OH- | D. | 苹果汁含有Fe3+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com