
| 操作 | 现象 | 结论 | |
| A | 先加硝酸,再滴加BaCl2溶液 | 产生白色沉淀 | 原溶液中一定有SO42- |
| B | 先加入H2O2溶液,再加KSCN溶液 | 溶液呈血红色 | 原溶液中一定有Fe2+ |
| C | 用洁净铂丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中一定有Na+、无K+ |
| D | 滴加NaOH溶液,加热,将湿润红色石蕊试纸置于试管口 | 试纸变蓝 | 原溶液中一定有NH4+ |
| A. | A | B. | B | C. | C | D. | D |
分析 A.生成的沉淀可能为氯化银,原溶液中可能含有银离子;
B.加入顺序颠倒,原溶液中可能含有Fe3+;
C.只能证明原溶液中含有钠离子,无法判断是否含有钾离子;
D.检验铵根离子时,先加入碱溶液加热,然后用红色石蕊试纸检验.
解答 解:A.先加硝酸,再滴加BaCl2溶液,生成的沉淀可能为AgCl,原溶液中可能含有Cl-,不一定含有SO42-,故A错误;
B.先加入H2O2溶液,再加KSCN溶液,无法排除原溶液中是否含有Fe3+,应该 先加入硫氰化钾溶液,溶液不变色,然后再加入双氧水,若溶液变为血红色,证明原溶液中含有Fe2+,故B错误;
C.用洁净铂丝蘸取溶液进行焰色反应,火焰呈黄色,证明原溶液中一定有Na+,无法判断原溶液中是否含有K+,故C错误;
D.滴加NaOH溶液,加热,将湿润红色石蕊试纸置于试管口,试纸变蓝,证明生成的气体为氨气,则原溶液中一定有NH4+,故D正确;
故选D.
点评 本题考查化学实验方案的评价,题目难度中等,明确常见离子的性质为解答关键,注意熟练掌握常见离子的检验方法,试题培养了学生的分析能力及逻辑推理能力.


科目:高中化学 来源: 题型:选择题
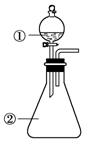 用如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )
用如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )| 选项 | ①中物质 | ②中物质 | 预测②中的现象 |
| A | 稀盐酸 | 碳酸钠与氢氧化钠的混合溶液 | 立即产生气泡 |
| B | 浓硝酸 | 用砂纸打磨过的铝条 | 产生红棕色气体 |
| C | 草酸溶液 | 高锰酸钾酸性溶液 | 溶液逐渐褪色 |
| D | 饱和氯化铁溶液 | 浓氢氧化钠溶液 | 溶液呈红褐色 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
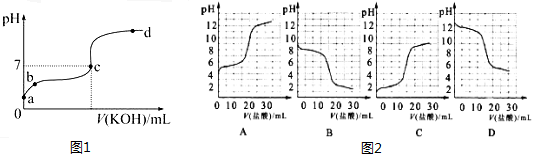
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入过量的NH3(g):Ag+、NH4+、NO3-、OH- | |
| B. | 加入过量 HNO3(aq):NH4+、Ag+、H+、NO3- | |
| C. | 通入过量 HCl(g):NH4+、H+、Cl-、NO3- | |
| D. | 加入过量NaOH(aq):NH4+、Na+、NO3-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇和浓硫酸混合加热至140℃,CH3CH2OH$→_{140℃}^{浓硫酸}$CH2=CH2↑+H2O | |
| B. | 1-溴丙烷与氢氧化钠的乙醇溶液供热:CH3CH2CH2Br+NaOH$→_{△}^{乙醇}$CH3CH2CH2OH+NaBr | |
| C. | 苯酚钠溶液中通入少量的CO2:2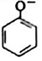 +H2O+CO2→2 +H2O+CO2→2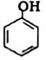 +CO${\;}_{3}^{2-}$ +CO${\;}_{3}^{2-}$ | |
| D. | 乙醛在碱性条件下被新制的氧化铜氧化:CH3CHO+2Cu(OH)2+OH-$\stackrel{△}{→}$CH3COO-+CuO↓+3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
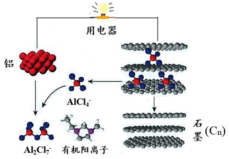 近期,科学家成功研制出一种可在一分钟内完成充放电的超常性能铝离子电池.该电池内部的A1Cl4-和有机阳离子构成电解质溶液,其放电工作原理如图所示.下列说法不正确的是( )
近期,科学家成功研制出一种可在一分钟内完成充放电的超常性能铝离子电池.该电池内部的A1Cl4-和有机阳离子构成电解质溶液,其放电工作原理如图所示.下列说法不正确的是( )| A. | 放电时,铝为负极、石墨为正极 | |
| B. | 充电时,A1Cl4-向石墨电极移动 | |
| C. | 放电时,负极的电极反应式为A1十7A1Cl4--3e-=4 A12Cl7- | |
| D. | 充电时,电子从石墨电极直接经导线流入铝电极,然后再经电解质溶液流回石墨电极 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氢氧化镍在乙醇的悬浊液中可发生如下反应生成单质镍的配合物:Ni(OH)2+5CH3NC═(CH3NC)4Ni+CH3NCO+H2O
氢氧化镍在乙醇的悬浊液中可发生如下反应生成单质镍的配合物:Ni(OH)2+5CH3NC═(CH3NC)4Ni+CH3NCO+H2O查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 性质 | 应用 |
| A | Na2O2与水、CO2反应 | 潜水艇O2的来源 |
| B | 单质镁有强还原性 | 镁合金作飞机材料 |
| C | 次氯酸及其盐具有漂白性 | 净化饮用水 |
| D | 铜不与O2反应 | 制备铜币 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com