
| A、50mL 2mol/LCaCl2溶液 |
| B、100mL 2mol/LNaCl溶液 |
| C、50mL 4mol/LCaCl2溶液 |
| D、100mL 1mol/LNaCl溶液 |


科目:高中化学 来源: 题型:
| A、HBr、HCl、BaSO4 |
| B、NH4Cl、CH3COOH、Cu |
| C、NaOH、CO2、NH3?H2O |
| D、HClO、Na2S、Ba(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、FeCl3溶液与Cu的反应:Cu+Fe3+=Cu2++Fe2+ | ||||
| B、NO2与水的反应:3NO2+H2O=2NO3-+2H++NO | ||||
| C、醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+=Ca2++H2O+CO2↑ | ||||
D、用铂电极电解氯化镁溶液:2Cl-+2H2O
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、大理石溶于醋酸中的反应:CaCO3+2H+=Ca2++H2O+CO2↑ |
| B、AlCl3溶液中加入过量的浓氨水:Al3++4NH3?H2O=AlO2-+4NH4++2H2O |
| C、用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+=Cu2++2Fe2+ |
| D、钠与水反应:Na+2H2O=Na++2OH-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
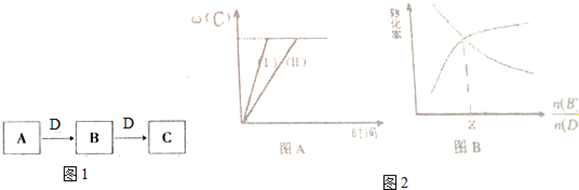
| 实验组 | 温度 | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| B | D | C | B | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| n(B) |
| n(D) |
查看答案和解析>>
科目:高中化学 来源: 题型:
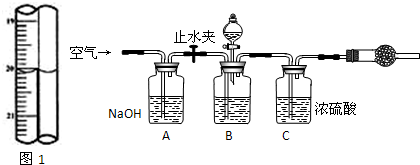
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com