
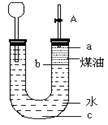
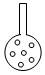
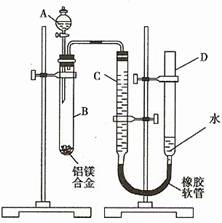
A.  打开右端胶塞,将一小块金属钠加入到煤油中,反应前片刻,钠的位置应在a处 打开右端胶塞,将一小块金属钠加入到煤油中,反应前片刻,钠的位置应在a处 |
B.开始反应后,能观察到的 实验现象是钠在b处液面以下的水中反应 实验现象是钠在b处液面以下的水中反应 |
| C.反应一段时间后,左端液面上升,进入长颈漏斗,a处有无色气体产生 |
| D.若用苯或酒精来代替煤油,可观察到相同的实验现象 |
 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
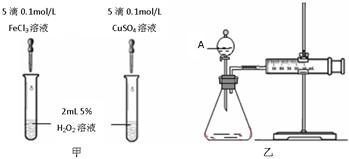
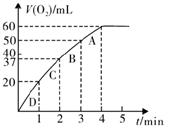
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| A.试样中含有加热不挥发的杂质 |
| B.试样中含有加热易挥发的杂质 |
| C.测试前试样已有部分脱水 |
| D.实验前坩埚未完全干燥 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
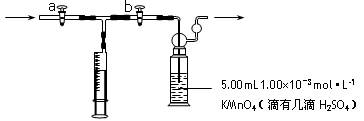
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
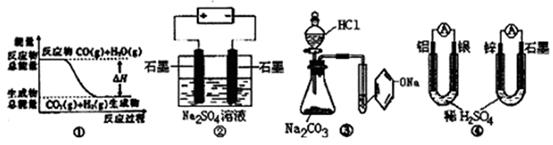
A.图①表示反应:CO(g)+H2O(g) CO2(g)+H2(g)中的△H>0 CO2(g)+H2(g)中的△H>0 |
| B.图②中通电时发生反应的化学方程式为:Na2SO4==2Na+SO2↑+O2↑ |
| C.装置③可做比较盐酸、碳酸、苯酚酸性强弱的实验 |
D.图④的两个装置中,铝电极和锌电极都是原 电池的负极 电池的负极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com