
| A. | 达平衡时,A2的正反应速率与B2的逆反应速率相等 | |
| B. | b≤0.2mol/L | |
| C. | 其它条件不变,在反应过程中使用了催化剂,可提高 A2、B2的转化率 | |
| D. | 该反应达平衡时气体物质的量浓度之和小于(a+b+0.3)mol/L |
分析 A、根据达平衡时,同种物质的正反应速率与逆反应速率相等判断;
B、根据可逆反应不可能反应到底分析平衡时B2的浓度为 b-0.2>0判断;
C、因为催化剂只改变反应速率,不改变平衡移动;
D、根据A2(g)+2B2(g)?2C(g),
起始浓度a b 0.3
转化浓度0.1 0.2 0.2
平衡浓度a-0.1 b-0.2 0.5
进行判断.
解答 解:根据A2(g)+2B2(g)?2C(g),
起始浓度a b 0.3
转化浓度0.1 0.2 0.2
平衡浓度a-0.1 b-0.2 0.5
A、达平衡时,A2的正反应速率与A2的逆反应速率相等,又B2的逆反应速率是A2的逆反应速率2倍,所以A2的正反应速率与B2的逆反应速率不相等,故A错误;
B、根据以上分析,可逆反应不可能反应到底,则平衡时B2的浓度为b-0.2>0,所以b>0.2,故B错误;
C、因为催化剂只改变反应速率,不改变平衡移动,故C错误;
D、根据以上分析,反应达平衡时气体物质的量浓度之和为a-0.1+b-0.2+0.5=a+b+0.2小于(a+b+0.3)mol/L,故D正确;
故选:D.
点评 本题考查了平衡移动的相关知识,根据可逆反应的特点及题中数据进行分析,本题难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
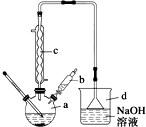 溴苯是一种常用的化工原料.实验室制备溴苯的实验步骤如下:
溴苯是一种常用的化工原料.实验室制备溴苯的实验步骤如下:| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 在水中的溶解度 | 微溶 | 微溶 | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 它的名称为( )
它的名称为( )| A. | 3,3-二甲基-2-乙基-戊烷 | B. | 3,3-二甲基-4-乙基戊烷 | ||
| C. | 2,3,3-三甲基戊烷 | D. | 3,3,4-三甲基己烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①③ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 W、X、Y和Z是常见的短周期元素,其原子半径随原子序数变化如图所示.己知W的一种核素的质量数为18,中子数为10;X和Ne的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期主族元素中最大.
W、X、Y和Z是常见的短周期元素,其原子半径随原子序数变化如图所示.己知W的一种核素的质量数为18,中子数为10;X和Ne的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期主族元素中最大.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
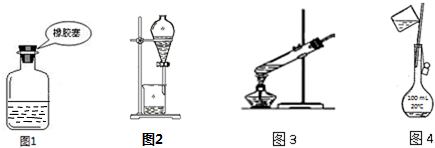
| A. | 图1装置:存放NaOH溶液 | |
| B. | 图2装置:分离乙酸乙酯和水 | |
| C. | 图3装置:葡萄糖的银镜反应 | |
| D. | 图4装置:配制 100 mL 1 mol/L NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 的烃,下列说法中正确的是( )
的烃,下列说法中正确的是( )| A. | 分子中至少有9个碳原子处于同一平面上 | |
| B. | 分子中至多有26个原子处于同一平面上 | |
| C. | 该烃能使酸性高锰酸钾溶液和溴的四氯化碳溶液褪色 | |
| D. | 该烃属于苯的同系物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com