
将一小块金属钠分别投入盛有:a.水、b.乙醇、c.稀H2SO4的三个小烧杯中,反应速率由快到慢的顺序为______________。解释反应速率不同的原因:__________________________。
科目:高中化学 来源: 题型:
自从1803年英国化学家、物理学家道尔顿提出了原子假说,人类对原子结构的认识就不断深入、发展,并通过实验事实不断地完善对原子结构的认识。下列关于原子结构模型的说法中,正确的是( )
A.道尔顿的原子结构模型将原子看作实心球,故不能解释任何问题
B.汤姆逊“葡萄干布丁”原子结构模型成功地解释了原子中的正负粒子是可以稳定共存的
C.卢瑟福核式原子结构模型指出了原子核和核外电子的质量关系、电性关系及占有体积的关系
D.玻尔电子分层排布原子结构模型引入了量子化的概念,能够成功解释所有的原子光谱
查看答案和解析>>
科目:高中化学 来源: 题型:
工业炼铝的流程
铝是地壳中含量最多的金属元素,在自然界主要以化合态形式存在于氧化铝中。铝土矿的主要成分是Al2O3,此外还含有少量SiO2、Fe2O3等杂质,冶炼金属铝很重要的一个过程是Al2O3的提纯。由于Al2O3是两性氧化物,而杂质SiO2是酸性氧化物,Fe2O3是碱性氧化物,因而可设计出两种提纯氧化铝的方案。
方案一:碱溶法
讨论回答下列问题:
(1)写出①、③两步骤中可能发生反应的离子方程式。
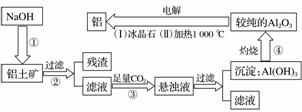
(2)步骤③中不用盐酸(或H2SO4)酸化的理由是__________________________。
(3)步骤④中得到较纯的Al2O3,可能含有________杂质,在电解时它不会影响铝的纯度的原因:________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中可能含有H+、NH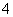 、Mg2+、Al3+、Fe3+、CO
、Mg2+、Al3+、Fe3+、CO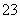 、SO
、SO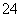 、NO
、NO 中的几种。①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则下列说法正确的是( )
中的几种。①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则下列说法正确的是( )
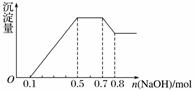
A.溶液中的阳离子只有H+、Mg2+、Al3+
B.溶液中n(NH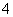 )=0.2 mol
)=0.2 mol
C.溶液中一定不含CO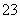 ,可能含有SO
,可能含有SO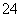 和NO
和NO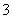
D.n(H+)∶n(Al3+)∶n(Mg2+)=1∶1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
镁在空气中燃烧除生成MgO外,还可能生成Mg3N2。某校化学兴趣小组的同学利用镁在空气中燃烧后的固体(不含单质)进行实验,探究其组成。
(1)甲组同学取一定量燃烧后的固体投入水中,得到了一种能使湿润的红色石蕊试纸变蓝的气体,该气体的化学式为____________________,说明固体中含有Mg3N2,生成该气体的化学方程式为________________________________________________________________________
________________________________________________________________________。
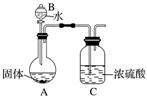
(2)乙组同学为测定Mg3N2的含量,用下图所示装置进行实验,充分反应后再加热A。其中浓硫酸的作用是___________________________,对A加热的目的是_______________________。
已知加入的固体质量为4.0 g,最终C装置增重a g,则固体中含Mg3N2______ g(用含a的式子表示)。
(3)丙组有的同学认为乙组同学的测定结果偏高,理由是_______________________。
有的同学认为乙组同学的测定结果偏低,理由是________________________。
丙组同学进行了改进,他们将乙组同学实验中得到的难溶固体进行过滤、洗涤、干燥,并灼烧固体至恒重,测得其质量为4.08 g。上述过程中,洗涤沉淀的操作是________________________________________________________________________
________________________________________________________________________。
镁在空气中燃烧后生成的固体中Mg3N2的质量分数为______________。
(4)有一种用铵盐与含镁矿石混合煅烧制取氧化镁的方法,解决了现有方法存在的原料成本高、项目投资大、能耗高、副产品不好用等问题,其原理是将含镁矿石粉(含氧化镁)与铵盐混合,经过煅烧、水溶、过滤,得到粗镁盐溶液,并回收煅烧产生的氨。写出用固体(NH4)2SO4与含镁矿石粉混合煅烧时的化学反应方程式__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
判断正误,正确的划“√”,错误的划“×”
(1)Na2O2与Na2O中均只存在离子键( )
(2)Na2O2与Na2O晶体中阳离子与阴离子的个数比均为2∶1( )
(3)2Na2O2+2H2O===4NaOH+O2↑
H2O既不是氧化剂也不是还原剂( )
(4)Na2O、Na2O2组成元素相同,与CO2反应产物也相同( )
(5)Na2O2的电子式为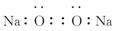 ( )
( )
查看答案和解析>>
科目:高中化学 来源: 题型:
下图表示某固态
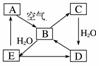
单质A及其化合物之间的转化关系(某些产物和反应条件已略去)。化合物B在常温常压下为气体,B和C的相对分子质量之比为4∶5,化合物D是重要的工业原料。
(1)写出A在加热条件下与H2反应的化学方程式:
________________________________________________________________________。
(2)写出E与A的氢化物反应生成A的化学方程式:
________________________________________________________________________。
(3)写出一个由D生成B的化学方程式:
________________________________________________________________________。
(4)将5 mL 0.10 mol·L-1的E溶液与10 mL 0.10 mol·L-1的NaOH溶液混合。
①写出反应的离子方程式:_____________________________;
②反应后溶液的pH________7(填“大于”、“小于”或“等于”),理由是________________________________________________________________________;
③加热反应后的溶液,其pH________(填“增大”、“不变”或“减小”),理由是________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com