
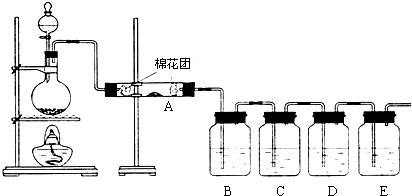
·ÖĪö ¢ń£®£Ø1£©Ģ¼ÓėÅØĮņĖįŌŚ¼ÓČČĢõ¼žĻĀ·“Ӧɜ³É¶žŃõ»ÆĢ¼”¢¶žŃõ»ÆĮņŗĶĖ®£¬¾Ż“ĖŠ“³ö·“Ó¦µÄ»Æѧ·½³ĢŹ½£»
£Ø2£©·“Ó¦ÓŠ¶žŃõ»ÆĮņ”¢¶žŃõ»ÆĢ¼ŗĶĖ®£¬ĶźĮĖ±ÜĆāøÉČÅ£¬Ó¦øĆĻČÓĆĪŽĖ®ĮņĖįĶ¾ßÓŠĖ®£¬Č»ŗóÓĆĘ·ŗģČÜŅŗ¾ßÓŠ¶žŃõ»ÆĮņ£¬ŌŁÓĆĖįŠŌøßĆĢĖį¼ŲČÜŅŗ³żČ„¶žŃõ»ÆĮņ”¢ÓĆĘ·ŗģČÜŅŗ¼ģŃ鶞Ńõ»ÆĮņŅŃ¾³ż¾”£¬×īŗóÓĆ³ĪĒåŹÆ»ŅĖ®¼ģŃ鶞Ńõ»ÆĢ¼£»
£Ø3£©µĪÓŠµķ·ŪµÄµāĖ®ĻŌĄ¶É«£¬¶žŃõ»ÆĮņÓėµ„ÖŹµā·“Ӧɜ³ÉĮņĖįŗĶµā»ÆĒā£»
¢ņ£®£Ø1£©¶žŃõ»ÆĮņÄܹ»ÓėĮņ»ÆĒā·“Ӧɜ³Éµ„ÖŹS£¬¶žŃõ»ÆĮņ±ķĻÖĮĖŃõ»ÆŠŌ£»
£Ø2£©ĖįŠŌøßĆĢĖį¼ŲČÜŅŗ¾ßÓŠĒæŃõ»ÆŠŌ£¬Äܹ»½«¶žŃõ»ÆĮņŃõ»Æ³ÉĮņĖį£¬øł¾Ż»ÆŗĻ¼Ū±ä»Æ·ÖĪö¶žŃõ»ÆĮņµÄŠŌÖŹ£»
£Ø3£©¶žŃõ»ÆĮņĪŖĖįŠŌŃõ»ÆĪļ£¬Äܹ»ÓėĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦£¬Ōņ¶žŃõ»ÆĮņĶØČėµĪÓŠ·ÓĢŖµÄNaOHČÜŅŗŗóČÜŅŗĶŹÉ«£®
½ā“š ½ā£ŗ¢ń£®£Ø1£©Ģ¼ÓėÅØĮņĖįŌŚ¼ÓČČĢõ¼žĻĀ·“Ó¦µÄ·½³ĢŹ½ĪŖ£ŗC+2H2SO4£ØÅØ£©$\frac{\underline{\;\;”÷\;\;}}{\;}$CO2”ü+2SO2”ü+2H2O£¬
¹Ź“š°øĪŖ£ŗC+2H2SO4£ØÅØ£©$\frac{\underline{\;\;”÷\;\;}}{\;}$CO2”ü+2SO2”ü+2H2O£»
£Ø2£©ÓÉÓŚČÜŅŗÖŠŗ¬ÓŠĖ®£¬ŅŖ¼ģŃé·“Ó¦²śĪļ£¬±ŲŠėĻČ¼ģŃéĖ®£¬Ź¹ÓĆŹŌ¼ĮĪŖĪŽĖ®CuSO4·ŪÄ©£»¶žŃõ»ÆĮņŗĶ¶žŃõ»ÆĢ¼¶¼Äܹ»Ź¹³ĪĒåŹÆ»ŅĖ®±ä»ė×Ē£¬ĖłŅŌÓ¦øĆĻČ¼ģŃ鶞Ńõ»ÆĮņ£¬Č»ŗ󽫶žŃõ»ÆĮņ³ż¾”£¬×īŗó¼ģŃ鶞Ńõ»ÆĢ¼£¬ĖłŅŌDÖŠĘ·ŗģČÜŅŗ²»ĶŹÉ«£¬Ö¤Ć÷¶žŃõ»ÆĮņŅŃ¾³ż¾”£»
¹Ź“š°øĪŖ£ŗĪŽĖ®CuSO4·ŪÄ©£»Ę·ŗģ²»ĶŹÉ«£»
£Ø3£©µĪÓŠµķ·ŪµÄµāĖ®ĻŌĄ¶É«£¬¶žŃõ»ÆĮņÓėµ„ÖŹµā·“Ӧɜ³ÉĮņĖįŗĶµā»ÆĒā£¬ĖłŅŌČÜŅŗŃÕÉ«±äĒ³£¬Ęä·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗSO2+I2+2H2O=SO42-+2I-+4H+£»
¹Ź“š°øĪŖ£ŗČÜŅŗĄ¶É«±äĒ³£»SO2+I2+2H2O=SO42-+2I-+4H+£»
¢ņ£®£Ø1£©¶žŃõ»ÆĮņÓėĮņ»ÆĒā·“Ӧɜ³ÉSµ„ÖŹ£¬¶žŃõ»ÆĮņÖŠSµÄ»ÆŗĻ¼Ū“Ó+4¼Ū½µĪŖ0¼Ū£¬¶žŃõ»ÆĮņ±ķĻÖĮĖŃõ»ÆŠŌ£¬ĖłŅŌÖ¤Ć÷SO2¾ßÓŠŃõ»ÆŠŌ£¬Ó¦øĆŌŚCÖŠ½ųČėĒāĮņĖį£»
¹Ź“š°øĪŖ£ŗĒāĮņĖį£»
£Ø2£©¶žŃõ»ÆĮņÖŠSµÄ»ÆŗĻ¼ŪĪŖ+4¼Ū£¬Äܹ»±»ĒæŃõ»Æ¼ĮĖįŠŌøßĆĢĖį¼ŲČÜŅŗŃõ»Æ³É+6¼Ū£¬·“Ó¦ÖŠ¶žŃõ»ÆĮņ±ķĻÖĮĖ»¹ŌŠŌ£»
¹Ź“š°øĪŖ£ŗ»¹Ō£»
£Ø3£©EÖŠ¼ÓČėµĪÓŠ·ÓĢŖµÄNaOHČÜŅŗ£¬ČÜŅŗ»įĶŹÉ«£¬Ö¤Ć÷¶žŃõ»ÆĮņÄܹ»ÓėĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦£¬Ōņ¶žŃõ»ÆĮņĪŖĖįŠŌŃõ»ÆĪļ£»
¹Ź“š°øĪŖ£ŗĖį£®
µćĘĄ ±¾Ģāæ¼²éĮĖÅØĮņĖįÓėC µÄ·“Ó¦£¬ĢāÄæÄѶČÖŠµČ£¬×¢ŅāÕĘĪÕÅØĮņĖįµÄ»ÆѧŠŌÖŹ£¬Äܹ»Éč¼ĘŹµŃé¼ģŃéC ÓėÅØĮņĖįµÄ·“Ó¦²śĪļ£¬Ć÷Č·¶žŃõ»ÆĮņ¾ßÓŠĘư׊Ō”¢»¹ŌŠŌ”¢Ńõ»ÆŠŌŹĒ½āĢāµÄ¹Ų¼ü£¬ŹŌĢā²ąÖŲ»ł“”ÖŖŹ¶µÄ漲飬ӊĄūÓŚĢįøßѧɜĮé»īÓ¦ÓĆ»ł“”ÖŖŹ¶µÄÄÜĮ¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģ¼ŖĮÖŹ”øßČżÉĻµŚ¶ž“ĪÄ£Äā»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
N2O¼ČŹĒŅ½Ń§ÉĻµÄŅ»ÖÖĀé×ķ¼Į£¬ÓÖŹĒŅ»ÖÖ³£¼ūµÄĪĀŹŅĘųĢ唣ÖĘČ”N2OµÄ·½·ØÓŠŗܶą£¬ĄżČē
¢ŁNH4NO3===N2O”ü£«2H2O
¢ŚK2SO3£«2NO===K2SO4£«N2O”ü
¢Ū2NH3£«2O2===N2O”ü£«3H2O
¢Ü2NaNO3£«£ØNH4£©2SO4===2N2O”ü£«Na2SO4£«4H2OµČ”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®·“Ó¦¢ŁÖŠĻõĖįļ§¼ČŹĒŃõ»Æ¼ĮÓÖŹĒ»¹Ō¼Į£¬H2OŹĒŃõ»Æ²śĪļ
B£®·“Ó¦¢ŚÖŠK2SO3ŹĒ»¹Ō¼Į£¬N2OŹĒŃõ»Æ²śĪļ
C£®·“Ó¦¢ŪÖŠĆæÉś³É1 mol N2O£¬×ŖŅĘ8 molµē×Ó
D£®·“Ó¦¢ÜÖŠNaNO3ŹĒ»¹Ō¼Į£¬N2O¼ČŹĒŃõ»Æ²śĪļÓÖŹĒ»¹Ō²śĪļ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğŌĘÄĻŹ”øßŅ»9ŌĀŌĀæ¼»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗ¼ņ“šĢā
£Ø1£©»šŅ©ŹĒÖŠ¹śµÄ”°ĖÄ“ó·¢Ć÷”±Ö®Ņ»£¬ÓĄŌ¶ÖµµĆŃ×»Ę×ÓĖļ½¾°Į£¬Ņ²ÓĄŌ¶»į¼¤Ąų×ÅĪŅĆĒČ„·Ü·¢Ķ¼Ē攣ŗŚ»šŅ©ŌŚ·¢Éś±¬ÕØŹ±£¬·¢ÉśČēĻĀµÄ·“Ó¦£ŗ2KNO3+C£«S===K2S+2NO2”ü+CO2”ü”£±»Ńõ»ÆµÄŌŖĖŲŹĒ £¬Ńõ»Æ¼ĮŹĒ £¬»¹Ō²śĪļŹĒ ”£µē×Ó×ŖŅʵÄ×ÜŹżĪŖ__________”£
£Ø2£©¹ś¼ŅĪĄÉś²æŌŚ2000ÄźĒ°¾Ķ¾ö¶ØÖš²½Ź¹ÓĆĪČ¶Ø”¢øߊ§”¢ĪŽ¶¾µÄ¶žŃõ»ÆĀČČ”“śĀČĘųĻū¶¾ŅūÓĆĖ®”£ŅŃÖŖ¶žŃõ»ÆĀČČÜÓŚĖ®Ź±ÓŠŃĒĀČĖįøłĄė×Ó£ØClO2-£©Éś³É£¬ĒŅŃõ»Æ²śĪļÓė»¹Ō²śĪļµÄĪļÖŹµÄĮæÖ®±ČĪŖ1”Ć1”£¶žŃõ»ÆĀČČÜÓŚĖ®µÄ·“Ó¦·½³ĢŹ½2ClO2 + H2O£½HClO3 + HClO2£¬ĒėÓƵ„ĻßĒűźĆ÷µē×Ó×ŖŅĘ·½ĻņŗĶŹżÄæ²¢Öø³öŃõ»Æ²śĪļ”£2ClO2 + H2O£½HClO3 + HClO2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ¶žŃõ»ÆĢ¼µÄ²¶×½ŗĶĄūÓĆŹĒĪŅ¹śÄÜŌ“ĮģÓņµÄŅ»øöÖŲŅŖÕ½ĀŌ·½Ļņ£®
¶žŃõ»ÆĢ¼µÄ²¶×½ŗĶĄūÓĆŹĒĪŅ¹śÄÜŌ“ĮģÓņµÄŅ»øöÖŲŅŖÕ½ĀŌ·½Ļņ£®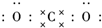 £¬Ėłŗ¬»Æѧ¼üµÄĄąŠĶŹĒ¹²¼Ū¼ü£®
£¬Ėłŗ¬»Æѧ¼üµÄĄąŠĶŹĒ¹²¼Ū¼ü£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
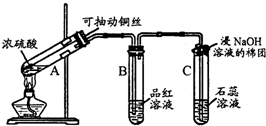
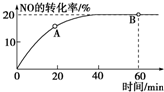 £Ø1£©Ä³ĪĀ¶ČĻĀ£¬ĻņČŻ»żĪŖ1LµÄČŻĘ÷ÖŠ³äČė3mol NOŗĶ1mol CO£¬·¢Éś2NO£Øg£©+2CO£Øg£©???N2£Øg£©+2CO2£Øg£©·“Ó¦£¬NOµÄ×Ŗ»ÆĀŹĖꏱ¼äµÄ±ä»ÆČēĶ¼ĖłŹ¾£®
£Ø1£©Ä³ĪĀ¶ČĻĀ£¬ĻņČŻ»żĪŖ1LµÄČŻĘ÷ÖŠ³äČė3mol NOŗĶ1mol CO£¬·¢Éś2NO£Øg£©+2CO£Øg£©???N2£Øg£©+2CO2£Øg£©·“Ó¦£¬NOµÄ×Ŗ»ÆĀŹĖꏱ¼äµÄ±ä»ÆČēĶ¼ĖłŹ¾£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| »ÆŗĻĪļ | Zn£ØOH£©2 | Fe£ØOH£©2 | Fe£ØOH£©3 |
| Ksp½üĖĘÖµ | 10-17 | 10-17 | 10-39 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
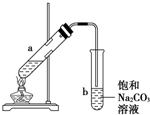 ČēĶ¼ĪŖŹµŃéŹŅÖĘȔɣĮæŅŅĖįŅŅõ„µÄ×°ÖĆĶ¼£¬ĻĀĮŠ¹ŲÓŚøĆŹµŃéµÄŠšŹöÖŠ£¬²»ÕżČ·µÄŹĒ£Ø””””£©
ČēĶ¼ĪŖŹµŃéŹŅÖĘȔɣĮæŅŅĖįŅŅõ„µÄ×°ÖĆĶ¼£¬ĻĀĮŠ¹ŲÓŚøĆŹµŃéµÄŠšŹöÖŠ£¬²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | ĻņaŹŌ¹ÜÖŠĻČ¼ÓČėŅŅ“¼£¬Č»ŗó±ßŅ”¶ÆŹŌ¹Ü±ßĀżĀż¼ÓČėÅØĮņĖį£¬ŌŁ¼Ó±ł“×Ėį | |
| B£® | ŹŌ¹ÜbÖŠµ¼Ęų¹ÜĻĀ¶Ė¹ÜæŚ²»ÄܽžČėŅŗĆęµÄŌŅņŹĒ·ĄÖ¹ŹµŃé¹ż³ĢÖŠ·¢Éśµ¹ĪüĻÖĻó | |
| C£® | ŹµŃ鏱¼ÓČČŹŌ¹ÜaµÄÄæµÄŹĒ¼°Ź±½«ŅŅĖįŅŅõ„Õō³ö²¢¼Óæģ·“Ó¦ĖŁĀŹ | |
| D£® | æɽ«±„ŗĶĢ¼ĖįÄĘČÜŅŗ»»³ÉĒāŃõ»ÆÄĘČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com