
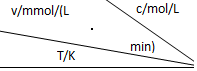
 | 0.600 | 0.500 | 0.400 | 0.300 |
| 318.2 | 3.60 | 3.00 | 2.40 | 1.80 |
| 328.2 | 9.00 | 7.50 | a | 4.50 |
| b | 2.16 | 1.80 | 1.44 | 1.08 |
| A�� | a=6.00 | |
| B�� | ��ͬ�¶�ʱ������Ũ�ȼ���һ�������ʱ����ͬ | |
| C�� | b��318.2 | |
| D�� | ͬʱ�ı䷴Ӧ�¶Ⱥ����ǵ�Ũ�ȣ�v���ܲ��� |
���� A���ɱ���֪�¶���318.2��328.2�棬��Ũ����ͬ�������$\frac{{v}_{318.2}}{{v}_{328.2}}$=0.4���ɴ˽��
B���¶�Խ�߷�Ӧ����Խ�죬��������Ũ�ȼ���һ�������ʱ�䲻ͬ���¶ȸߵ�����ʱ��̣�
C���ɱ���֪�¶���328.2���b����Ũ����ͬ������£�ˮ�����ʱ�С�������¶Ƚ��ͣ�
D���ɱ���֪�¶���318.2���b��Ũ����0.3mol/L��0.5mol/L��������ȣ�
��� �⣺A���ɱ���֪�¶���318.2��328.2�棬��Ũ����ͬ�������$\frac{{v}_{318.2}}{{v}_{328.2}}$=0.4������a=$\frac{2.4}{0.4}$=6����A��ȷ��
B���¶�Խ�߷�Ӧ����Խ�죬��������Ũ�ȼ���һ�������ʱ�䲻ͬ���¶ȸߵ�����ʱ��̣���B����
C���ɱ���֪�¶���328.2���b����Ũ����ͬ������£�ˮ�����ʱ�С�������¶Ƚ��ͣ������¶�b��318.2����C��ȷ��
D���ɱ���֪�¶���318.2���b��Ũ����0.3mol/L��0.5mol/L��������ȣ�����1.80������v���ܲ��䣬��D��ȷ��
��ѡB��
���� ���⿼����ۺϣ��漰��Ӧ���ʼ��㡢Ӱ�����ʵ����ط����ȣ�����ѧ���������ݷ��������������Ŀ��飬ע�ضԸ߿���Ƶ�����ѵ������Ŀ�Ѷ��еȣ�


 ���ѵ����Ԫ��ĩ���100��ϵ�д�
���ѵ����Ԫ��ĩ���100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ�Ӱ뾶��W��X��Y��Z | |
| B�� | ���ԣ�W�ĺ�����ǿ��Z�ĺ����� | |
| C�� | �ȶ��ԣ�Z����̬�⻯��ǿ��Y��̬�⻯�� | |
| D�� | X��Z�γɻ�����һ�������ӻ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 8.0gCu2S��CuO�Ļ�����к���ͭԭ����Ϊ0.1NA | |
| B�� | ���³�ѹ�£�3.0g�����к��е�̼�����Ϊ0.07NA | |
| C�� | 250mL 1 mol•L-1H2SO4��Һ�к�����ԭ����ΪNA | |
| D�� | ��⾫��ͭʱ���������ܽ�32gͭ����ת�Ƶĵ�����ΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ������ | X�Լ� | ���ӷ���ʽ |
| A | K+��Na+��ClO-��SO42- | ����SO2 | SO2+ClO-+H2O�TSO42-+Cl-+2H+ |
| B | NH4+��Fe3+��Br-��SO42- | ����H2S | 2Fe3++H2S�T2Fe2++S��+2H+ |
| C | NH4+��Na+��Fe3+��AlO2- | ����ͭ�� | 2Fe3++Cu�T2Fe2++Cu2+ |
| D | K+��Na+��HCO3-��AlO2- | ����HCl | H++AlO2-+H2O�TAl��OH��3�� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
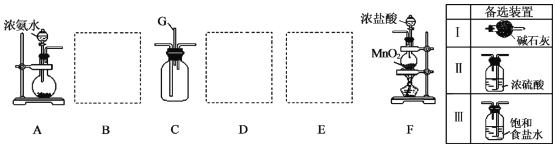
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO2��H2S | B�� | H2O2��C3H6 | C�� | C2H4��CH4 | D�� | NH3��HCl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
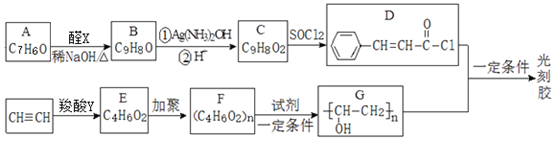
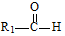 +
+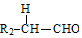 $��_{��}^{ϡNaOH}$
$��_{��}^{ϡNaOH}$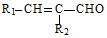 ��R1��R2Ϊ�������⣩
��R1��R2Ϊ�������⣩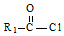 +R2OH$\stackrel{һ������}{��}$
+R2OH$\stackrel{һ������}{��}$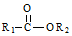 +HCl��R1��R2Ϊ������
+HCl��R1��R2������ ��
�� ��
��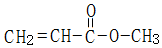
 ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com