
【题目】标出下列氧化还原反应过程中有关变化
(1)用单线桥标出电子的转移方向和数目 ,其中氧化剂是 .
NO+N O2+2NaOH═2NaN O2+H2O
(2)用双线桥标出化合价的变化,其中还原剂与氧化剂的物质的量比值是 .
2MnO4﹣+8H++5S O2═2Mn2++5SO42﹣+4H2O.
【答案】
(1)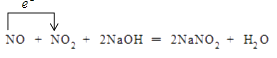 ;NO2
;NO2
(2)5:2
【解析】解:(1)反应NO+NO2+2NaOH═2NaNO2+H2O中,只有N元素化合价发生变化,N元素化合价分别由+2价、+4价变化为+3价,化合价降低值=化合价升高值=转移电子数=1,电子转移方向和数目为: 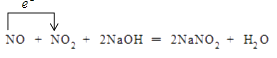 ,NO2得到电子被还原,NO2做氧化剂,
,NO2得到电子被还原,NO2做氧化剂,
所以答案是: 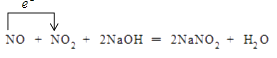 ;NO2;(2)反应2MnO4﹣+8H++5SO2═2Mn2++5SO42﹣+4H2O中,Mn元素化合价由+7价降低到+2价,被还原,MnO4﹣得电子为氧化剂,S元素化合价由+4价升高到+6价,被氧化,SO2失电子为还原剂,还原剂与氧化剂的物质的量之比为 5:2,氧化剂和还原剂得失电子数目相等,由元素化合价的变化可知转移的电子数目为10,用“双线桥法”表示氧化还原反应中电子转移情况为:
;NO2;(2)反应2MnO4﹣+8H++5SO2═2Mn2++5SO42﹣+4H2O中,Mn元素化合价由+7价降低到+2价,被还原,MnO4﹣得电子为氧化剂,S元素化合价由+4价升高到+6价,被氧化,SO2失电子为还原剂,还原剂与氧化剂的物质的量之比为 5:2,氧化剂和还原剂得失电子数目相等,由元素化合价的变化可知转移的电子数目为10,用“双线桥法”表示氧化还原反应中电子转移情况为: 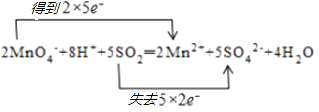 ,
,
所以答案是: 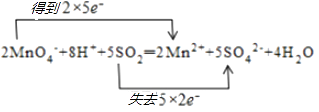 ;5:2.
;5:2.


 步步高达标卷系列答案
步步高达标卷系列答案科目:高中化学 来源: 题型:
【题目】某小组同学为探究物质的氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)。
已知:①溴水为溴的水溶液,溴水为橙黄色,溴蒸气为红棕色,均有毒
②氯水为氯气的水溶液。
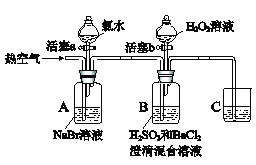
实验记录如下:
实验操作 | 实验现象 | |
Ⅰ | 打开活塞a,滴加氯水,关闭活塞a | A中溶液变为橙黄色 |
Ⅱ | 吹入热空气 | A中橙黄色明显变浅;B中有气泡,产生大量白色沉淀,混合液颜色无明显变化 |
Ⅲ | 停止吹入空气,打开活塞b,逐滴加入H2O2溶液 | 开始时颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成橙黄色 |
请回答下列问题:
(1)A中反应的离子方程式是__________________________________________。
(2)实验操作II吹入热空气的目的是___________________________________。
(3)装置C的作用是_____________________________________。
(4)实验操作III,混合液逐渐变成橙黄色,其对应的离子方程式是____________。
(5)由操作I得出的结论是_____________,由操作III得出的结论是______________。
(6)实验反思:实验操作III,开始时颜色无明显变化的原因是(写出一条即可):___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于盐酸与醋酸两种稀溶液的说法正确的是( )
A 相同浓度的两溶液中c(H+)相同
B 100mL 0.1mol/L的两溶液能中和等物质的量的氢氧化钠
C pH=3的两溶液稀释100倍,pH都为5
D 两溶液中分别加人少量对应的钠盐,c(H+)均明显减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用锌,氧化铜,稀硫酸作原料制取铜时,有下列两种途径:
(1)锌 ![]() 氢气
氢气 ![]() 铜
铜
(2)氧化铜 ![]() 硫酸铜
硫酸铜 ![]()
若用这两种方法制得相同质量的铜时,下列叙述符合实际实验结果的是( )
A.消耗相同质量的硫酸
B.消耗相同质量的锌
C.消耗相同质量的氧化铜
D.生成的硫酸锌质量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 阳离子只有氧化性,阴离子只有还原性
B. 含氧酸可作氧化剂,而无氧酸不能
C. 在8NH3+3Cl2===N2+6NH4Cl反应中,氧化剂与还原剂分子个数之比是2:3
D. 已知还原性:Fe2+>Br-,可知反应2Fe3++2Br-===2Fe2++Br2不易进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为鉴别卤代烃中所含卤素原子,现有下列实验操作步骤,正确的顺序是( ) ①加入AgNO3溶液②加入少许卤代烃试样③加热 ④加入5mL 4molL﹣1 NaOH溶液⑤加入5mL 4molL﹣1 HNO3溶液.
A.②④③①⑤
B.②③①④⑤
C.②④③⑤①
D.②⑤③①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 34 g H2O2中含原子总数为4NA
B. 2.4g金属镁变成镁离子时得到的电子数目为0.2NA
C. 若气体的摩尔体积为22.4 L/mol,则所处条件一定为标准状况
D. 摩尔是用来衡量微观粒子多少的一种物理量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,向一定体积0.1molL﹣1的醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液pOH[pOH=﹣lgc(OH﹣)]与pH的变化关系如图所示,则( ) 
A.N点处pH>pOH,则N点处所示溶液呈酸性
B.该温度下水的离子积Kw=1×10﹣2a
C.Q点所示溶液呈中性,则M,N,Q三点中只有Q点溶液中水的电离出的c(H+)与水的电离c(OH﹣)相等
D.M点所示溶液的导电能力强于Q
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com