
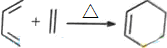 .根据下列转化流程,回答问题:
.根据下列转化流程,回答问题: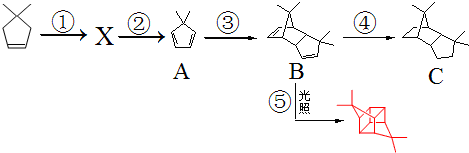
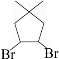 .
.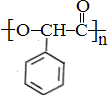 的合成路线:
的合成路线: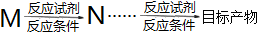 )
)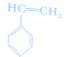 $\stackrel{Br_{2}}{→}$
$\stackrel{Br_{2}}{→}$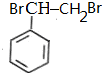 $→_{△}^{NaOH溶液}$
$→_{△}^{NaOH溶液}$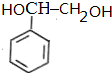 $\stackrel{[O]}{→}$
$\stackrel{[O]}{→}$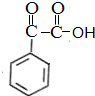 $→_{催化剂}^{H_{2}}$
$→_{催化剂}^{H_{2}}$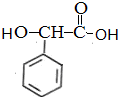 $\stackrel{浓H_{2}SO_{4}△}{→}$
$\stackrel{浓H_{2}SO_{4}△}{→}$ .
. 分析 根据题中各物质转化关系,比较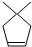 和A的结构简式可知,
和A的结构简式可知, 与溴加成生成X为
与溴加成生成X为 ,X在氢氧化钠醇溶液中加热发生消去反应生成A,A发生题中信息中的加成反应生成B,反应条件为加热,B再与氢气发生加成得C,B发生分子内加成得
,X在氢氧化钠醇溶液中加热发生消去反应生成A,A发生题中信息中的加成反应生成B,反应条件为加热,B再与氢气发生加成得C,B发生分子内加成得 ,制备
,制备 ,可以用B的芳香烃的同分异构体的同系物为
,可以用B的芳香烃的同分异构体的同系物为 ,由苯乙烯与溴加成,再水解得二元醇,再氧化得
,由苯乙烯与溴加成,再水解得二元醇,再氧化得 ,
, 与氢气加成得
与氢气加成得 ,再发生加聚反应得
,再发生加聚反应得 ,据此答题;
,据此答题;
解答 解:根据题中各物质转化关系,比较 和A的结构简式可知,
和A的结构简式可知, 与溴加成生成X为
与溴加成生成X为 ,X在氢氧化钠醇溶液中加热发生消去反应生成A,A发生题中信息中的加成反应生成B,反应条件为加热,B再与氢气发生加成得C,B发生分子内加成得
,X在氢氧化钠醇溶液中加热发生消去反应生成A,A发生题中信息中的加成反应生成B,反应条件为加热,B再与氢气发生加成得C,B发生分子内加成得 ,
,
(1)根据上面的分析可知,反应②的条件为NaOH醇溶液,加热,反应③的条件为加热,
故答案为:NaOH醇溶液,加热; 加热;
(2)根据上面的分析可知,反应①为加成反应,反应⑤为加成反应,
故答案为:加成;加成;
(3)X为 ,
,
故答案为: ;
;
(4)制备 ,可以用B的芳香烃的同分异构体的同系物为
,可以用B的芳香烃的同分异构体的同系物为 ,由苯乙烯与溴加成,再水解得二元醇,再氧化得
,由苯乙烯与溴加成,再水解得二元醇,再氧化得 ,
, 与氢气加成得
与氢气加成得 ,再发生加聚反应得
,再发生加聚反应得 ,合成路线为
,合成路线为 $\stackrel{Br_{2}}{→}$
$\stackrel{Br_{2}}{→}$ $→_{△}^{NaOH溶液}$
$→_{△}^{NaOH溶液}$ $\stackrel{[O]}{→}$
$\stackrel{[O]}{→}$ $→_{催化剂}^{H_{2}}$
$→_{催化剂}^{H_{2}}$ $\stackrel{浓H_{2}SO_{4}△}{→}$
$\stackrel{浓H_{2}SO_{4}△}{→}$ ,
,
故答案为: $\stackrel{Br_{2}}{→}$
$\stackrel{Br_{2}}{→}$ $→_{△}^{NaOH溶液}$
$→_{△}^{NaOH溶液}$ $\stackrel{[O]}{→}$
$\stackrel{[O]}{→}$ $→_{催化剂}^{H_{2}}$
$→_{催化剂}^{H_{2}}$ $\stackrel{浓H_{2}SO_{4}△}{→}$
$\stackrel{浓H_{2}SO_{4}△}{→}$ .
.
点评 本题考查有机物推断与合成,侧重考查分析、推断、知识迁移能力,答题时注意结合题给信息解答,有机合成是本题的难点.


 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案科目:高中化学 来源: 题型:选择题
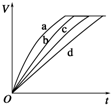 等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生氢气体
等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生氢气体| 组别 | c(HCl)/(mol•L-1) | 温度/(℃) | 状态 |
| 1 | 2.0 | 30 | 块状 |
| 2 | 2.5 | 30 | 块状 |
| 3 | 2.0 | 20 | 块状 |
| 4 | 2.5 | 30 | 粉末状 |
| A. | 4、3、2、1 | B. | 4、2、1、3 | C. | 3、4、2、1 | D. | 4、1、2、3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | K | L | M | Q | R | T | N |
| 原子半径/nm | 0.183 | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 | 0.152 |
| 主要化合价 | +1 | +2 | +3 | +6、-2 | +2 | -2 | +1 |
| A. | K、L、M三种元素的金属性逐渐减弱 | |
| B. | 在RCl2分子中,各原子均满足8电子的稳定结构 | |
| C. | Q元素的最高价氧化物为非电解质,其水溶液能够导电 | |
| D. | K在T单质中燃烧所形成的化合物中含有非极性共价键和离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 当今世界,能源的发展日益成为全世界、全人类共同关心的问题.
当今世界,能源的发展日益成为全世界、全人类共同关心的问题.| 电离能(kJ/mol) | I1 | I2 | I3 | I4 |
| A | 899 | 1 757 | 14 840 | 21 000 |
| B | 738 | 1 451 | 7 733 | 10 540 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 配制CuCl2溶液时,将CuCl2(s)溶于浓HCl后再加水冲稀,浓盐酸作用:有利于抑制CuCl2水解,可防止Cu(OH)2的形成 | |
| B. | 加热MnO2的浓HCl溶液制取氯气.浓盐酸作用:有利于减少氯气的溶解损失 | |
| C. | 浓硝酸不能溶解金,需用浓HCl溶液配制王水才能溶解金.浓盐酸作用:有利于增强Au的还原性,并且提高硝酸的氧化性 | |
| D. | 将浓硫酸滴入浓盐酸中制备HCl气体.浓盐酸作用:增大溶质的浓度,有利于促进平衡向气体溶解的逆方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 化学反应及其离子方程式 | 评价 |
| A | Fe3O4与过量稀硝酸反应:Fe3O4+8H+→2Fe3++Fe2++4H2O | 正确 |
| B | 在复盐NH4Fe(SO4)2溶液中逐滴加入Ba(OH)2溶液: 2Fe3++3SO42-+3Ba2++6OH-→3BaSO4↓+2Fe(OH)3↓ | 正确 |
| C | 在稀氨水中通入过量CO2:NH3•H2O+CO2→NH4++HCO3- | 正确 |
| D | FeBr2溶液与等物质的量的Cl2反应: 2Fe2++2Br-+2Cl2→2Fe3++4Cl-+Br2 | 错误,Fe2+与Br-的化学计量数之比应为1:2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | ||
| Y | Z | W |
| A. | X、Z、W的简单氢化物的稳定性Z>W>X | |
| B. | X元素的单质在化学反应中只表现还原性 | |
| C. | X、Y的简单离子半径Y>X | |
| D. | Y、Z、X的最高价氧化物均能与NaOH溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | 有关信息 |
| A | 其氢化物水溶液呈碱性 |
| B | 地壳中含量最多的元素 |
| C | 单质须保存在煤油中 |
| D | 单质与NaOH溶液反应可用于生产漂白液 |
| E | 单质是生活中用量最大的金属,其制品在潮湿空气中易被腐蚀或损坏 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 质量数 | B. | 中子数 | C. | 核电荷数 | D. | 能层和能级 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com