
设 NA 为阿伏加德罗常数,下列说法正确的是( )
A.标准状况下,0.1 mol Cl2 溶于水,转移的电子数目为0.1NA
B.物质的量浓度为0.1mol·L-1的MgCl2溶液中,含有Cl-个数为0.2NA
C.标准状况下,2.24L甲醇中含有C—H键的数目为0.3NA
D.常温下,22g CO2和N2O混合气体中,含有的原子数目为1.5NA
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案科目:高中化学 来源:2015届浙江省高三10月月考化学试卷(解析版) 题型:选择题
如图装置进行实验,将液体A逐滴加入到固体B中,下列叙述正确的是
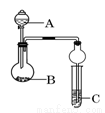
A.若A为浓氨水,B为生石灰,C中盛AlCl3溶液,则C中先产生白色沉淀后沉淀溶解
B.若A为浓硫酸,B为炭,C中盛有品红溶液,则C中溶液红色褪色
C.若A为浓硝酸,B为金属铜,C中盛有淀粉KI溶液,则C中溶液变蓝
D.若A为浓盐酸,B为MnO2,C中盛石蕊试液,则C中溶液先变红后褪色
查看答案和解析>>
科目:高中化学 来源:2015届河南省10月联考化学试卷(解析版) 题型:选择题
下列说法中,正确的有( )
(1)明矾可用于水的消毒净化;碳酸钡不可用于钡餐透视
(2)氮氧化物和碳氢化合物是构成光化学烟雾的重要物质
(3)氨常用作制冷剂,是因为其沸点极低,很容易液化
(4)硅的提纯与应用,促进了半导体元件与集成芯片的发展,可以说“硅是信息技术革命的催化剂”
(5)在硫酸亚铁铵的制备实验中,为了得到硫酸亚铁铵晶体,应小火加热蒸发皿,直到有大量晶体析出时停止加热
(6)通电时,溶液中溶质粒子分别向两极移动,胶体中胶粒向某一极移动
(7)铝粉和氧化镁粉末混合,高温能发生铝热反应
(8)高纯度的二氧化硅广泛用于制作光导纤维,光导纤维遭遇强碱会“断路”
(9)可用稀盐酸、碳酸钠溶液、硅酸钠溶液设计实验来验证氯、碳、硅三种元素的非金属性
(10)同主族元素的简单阴离子还原性越强,水解程度越大
(11)Al2O3在工业上用于制作耐高温材料,也用于电解法治炼铝
(12)在硫酸铜结晶水含量测定实验中,至少要用天平称量三次质量
(13)将水蒸汽通过灼热的铁粉,粉末变红,说明铁在高温条件下可与水发生化学反应
(14)先取少量试液于试管中,再加入氢氧化钠溶液,将润湿的红色石蕊试纸放在试管口,红色石蕊试纸不变蓝,证明溶液中不含铵根离子。
(15)已知次磷酸(H3PO2)是一元中强酸,则NaH2PO2是正盐
A.8句 B.6句 C.5句 D.7句
查看答案和解析>>
科目:高中化学 来源:2015届河南省洛阳市高三上学期期中考试化学试卷(解析版) 题型:选择题
为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作:
①过滤 ②加过量NaOH溶液 ③加适量盐酸 ④加过量Na2CO3溶液 ⑤加过量BaCl2溶液.
不正确的操作顺序是
A.⑤②④①③ B.④②⑤①③
C.②⑤④①③ D.⑤④②①③
查看答案和解析>>
科目:高中化学 来源:2015届河南省洛阳市高三上学期期中考试化学试卷(解析版) 题型:选择题
Na2O、NaOH、Na2CO3、NaCl、Na2SO4可按某种标准划为统一类物质,下列分类标准正确的是
①钠的化合物 ②能与硝酸反应的物质 ③可溶于水的物质 ④电解质 ⑤钠盐 ⑥钠的含氧化合物
A.①③④⑤ B.①②⑤⑥ C.①③④ D.②⑤⑥
查看答案和解析>>
科目:高中化学 来源:2015届河南省洛阳市高三上学期期中考试化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.化石燃料燃烧产生大量CO2,会导致温室效应
B.血液透析利用了胶体的性质
C.自来水可用氯气来杀菌消毒,说明氯气无毒
D.采用原煤脱硫技术,可减少燃煤燃时产生的SO2
查看答案和解析>>
科目:高中化学 来源:2015届河南省高三9月第二次阶段考化学试卷(解析版) 题型:选择题
下列反应与Na2O2+SO2→Na2SO4相比较,Na2O2的作用相同的是
A.2Na2O2+CO2→2Na2CO3+O2 B.2Na2O2+2SO3→2Na2SO4+O2
C.Na2O2+H2SO4→Na2SO4+H2O2 D.3Na2O2+Cr2O3→2Na2CrO4+Na2O
查看答案和解析>>
科目:高中化学 来源:2014-2015学年陕西省高三上学期期中理综化学试卷(A)(解析版) 题型:填空题
(14分) NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:2NaNO2+4HI===2NO↑+I2+2NaI+2H2O。
(1)上述反应中氧化剂是________。
(2)根据上述反应,鉴别NaNO2和NaCl。可选用的物质有:①水、②碘化钾淀粉试纸、③淀粉、④白酒、⑤食醋,你认为必须选用的物质有________(填序号)。
(3)某厂废液中,含有2%~5%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是________(填编号)。
A.NaCl B.NH4Cl C.HNO3 D.浓H2SO4
(4)请完成并配平以下化学方程式:
□Al+□NaNO3+□NaOH===□NaAlO2+□N2↑+□ 。
若反应过程中转移5 mol e-,则生成标准状况下N2的体积为________L。
(5)在微生物作用的条件下, NH4+经过两步反应被氧化成NO3ˉ。两步反应的能量变化示意图如下:

①第一步反应是 反应(填“放热”或“吸热”),
②1mol NH4+(aq)全部氧化成NO3ˉ(aq)的热化学方程式是: 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省莆田市高三上学期第二次月考化学试卷(解析版) 题型:填空题
(12分)A~G各物质间的关系如图,其中B、D为气态单质。

请回答下列问题:
(1)物质C、E分别为 、 。(填名称)
(2)反应①可选用不同的A进行,若反应在常温下进行,其化学方程式为 。
(3)反应②的离子方程式为 。
(4)新配制的F溶液应加入________以防止其转化为G。请设计实验检验F、G的混合溶液中F的金属阳离子。(写出试剂、操作、现象、结论) 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com