
(化学---选修3:物质结构和性质)锂—磷酸氧铜电池正极的的活性物质是Cu4O(PO4)2,可通过下列反应制备:2Na3PO4+4CuSO4+2NH3·H2O=Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O
(1)写出基态Cu2+的核外电子排布式:____________,与Cu同周期的元素中,与铜原子最外层电子数相等的元素还有___________(填元素符号),上述方程式中涉及到的N、O元素第一电离能由小到大的顺序为________________。
(2)PO43-的空间构型是___________。
(3)与NH3具有相同空间构型和键合形成的分子或离子有_________、___________(各举一例)
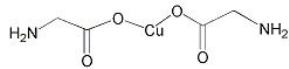
(4)氨基乙酸铜的分子结构如图,氮原子的杂化方式为______________。
(5)在硫酸铜溶液中加入过量KCN,生成配合物[Cu(CN)4]2-,则1molCN-中含有的π键的数目为___________。
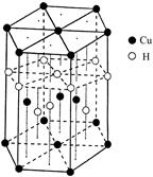
(6)Cu元素与H元素可形成一种红色化合物,其晶体结构单元如图所示。则该化合物的化学式
为______________________。
(7)铜晶体为面心立方最密堆积,铜的原子半径为127.8pm,列出晶体铜的密度表达式____________。
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2016-2017学年广西柳州铁路一中高二上段考理化学卷(解析版) 题型:选择题
下列物质在常温下发生水解时,对应的离子方程式正确的是( )
①Na2CO3:CO32-+2H2O H2O+CO2
H2O+CO2 ↑+2OH-
↑+2OH-
②NH4Cl:NH4++H2O NH3·H2O+H+
NH3·H2O+H+
③CuSO4:Cu2++2H2O Cu(OH)2+2H+
Cu(OH)2+2H+
④ NaF:F-+H2O
NaF:F-+H2O HF+OH-
HF+OH-
A.①④ B.②③ C.①③ D.②④
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省、醴陵四中高二上期中化学卷(解析版) 题型:选择题
将1 mol X、3 mol Y充入一个密闭容器中,在一定条件下发生如下反应并达到平衡:X(g) +3Y(g)  2Z(g);ΔH<0。当改变某个条件并达到新平衡后,下列叙述正确的是 ( )
2Z(g);ΔH<0。当改变某个条件并达到新平衡后,下列叙述正确的是 ( )
A.升高温度,X的体积分数减小
B.缩小体积,Y的物质的量浓度不变
C.保持容器体积不变,充入1mol的稀有气体He,Z的浓度不变
D.保持容器体积不变,充入2mol的Z(g),X的体积分数增大
查看答案和解析>>
科目:高中化学 来源:2017届四川省高三上综合测试三化学卷(解析版) 题型:填空题
[化学——选修3:物质结构与性质]N、P、As都是同主族的元素。
(1)As基态原子的电子排布式为 。和砷位于同一周期,且未成对电子数也相同的元素还有 种。
(2)元素周期表中,与P紧邻的4种元素中电负性最强的是 (填元素符号),Si、P、S三元素第一电离能由大到小的顺序为 。
(3)NH3、PH3、AsH3三者的空间构型相同,都是 ,它们的沸点由高到低的顺序为 (填化学式)
(4)白磷是由P4分子形成的分子晶体,每个P4分子是正四面体结构(如图)。
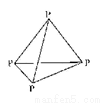
P的杂化方式为 。白磷易溶于CS2,难溶于水,原因是 。
(5)采用GaxIn(1-x)As(镓铟砷)等材料,可提高太阳能电池的效率。GaxIn(1-x)As立方体形晶胞中每1个顶点和面心都有1个原子,晶胞内部有4个原子,则该晶胞中含有 个砷原子。
查看答案和解析>>
科目:高中化学 来源:2017届四川省高三上综合测试三化学卷(解析版) 题型:选择题
分别进行下列操作,由现象得出的结论正确的是( )
选项 | 操作 | 现象 | 结论 |
A | 滴加Ba(NO3)2和HNO3混合溶液 | 生成白色沉淀 | 原溶液中有SO42- |
B | 将乙烯通入溴水中 | 溴水褪色 | 乙烯与溴水发 |
C | 分别将少量钠投入到盛有水和乙醇的烧杯中 | 盛水烧杯中反应剧烈 | 水中的氢比乙醇中的氢活泼性强 |
D | 滴加NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH |
查看答案和解析>>
科目:高中化学 来源:2017届陕西西安市高三上模拟三化学试卷(解析版) 题型:选择题
A、B、C、D是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,辛是由C元素形成的单质。已知:甲+乙=丁+辛,甲+丙=戊+辛;常温下0.1mol/L丁溶液的pH为13,下列说法正确的是
A. 元素C形成的单质可以在点燃条件分别与元素A、B、D形成的单质化合,所得化合物均存在共价键
B. 元素B、C、D的原子半径由大到小的顺序为:r(D) > r(C) > r(B)
C. 1.0 L 0.1 mol/L戊溶液中含阴离子总的物质的量小于0.1 mol
D. 1 mol甲与足量的乙完全反应共转移约1.204 × 1024个电子
查看答案和解析>>
科目:高中化学 来源:2017届陕西省高三上期中化学试卷(解析版) 题型:填空题
[化学——选修3:物质结构与性质]第四周期 过渡元素Fe、Ti可与C、H、N、O形成多种化合物。
过渡元素Fe、Ti可与C、H、N、O形成多种化合物。
(1)①H、C、N、O四种元素的电负性由小到大的顺序为 。
②下列叙述不正确的是 。(填字母)
A.因为HCHO与水分子间能形成氢键,所以CH2O易溶于水
B.HCHO和CO2分子中的中心原子均采用sp2杂化
C.C6H6分子中含有6个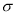 键和1个大
键和1个大 键,C2H2是非极性分子
键,C2H2是非极性分子
D.CO2晶体的熔点、沸点都比二氧化硅晶体的低
③氰酸(HOCN)是一种链状分子,它与异氰酸(HNCO)互为同分异构体,其分子内各原子最外层均已达到稳定结构,试写出氰酸的结构式 。
(2) Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物。
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是
②六氰合亚铁离子[Fe(CN)6]4 -中不存在 。
A、共价键
B、非极性键
C、配位键
D、σ键
E、π键
写出一种与 CN- 互为等电子体的单质分子式 。
(3)根据元素原子的外围电子排布特征,可将周期表分成五个区域,其中Ti属于 区。
(4)一种Al-Fe合金的立体晶胞如下图所示。请据此回答下列问题:
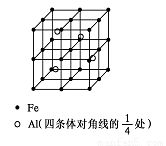
① 确定该合金的化学式 。
②若晶体的密度=ρ g/cm3,则此合金中最近的两个Fe原子之间的距离(用含ρ的代数式表示,不必化简)为 cm。
查看答案和解析>>
科目:高中化学 来源:2017届陕西省高三上期中化学试卷(解析版) 题型:选择题
①热分解法、②热还原法、③电解法是工业上制取金属的三种常用方法。下列金属与冶炼方法相对应的是( )
选项 | 金属 | 冶炼方法 |
A | K、Na | ③ |
B | Ca、Cu | ② |
C | Fe、Mg | ③ |
D | Al、Hg | ① |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省南京市高二上学期期中化学试卷(解析版) 题型:选择题
饮用水的消毒剂有多种,其中杀菌能力强且不影响水质的理想消毒剂是
A.液氯 B.臭氧 C.漂白粉 D.石灰
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com