
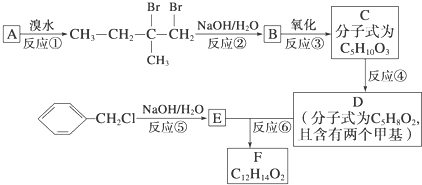
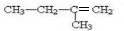 ,反应②是水解反应,生成物B为
,反应②是水解反应,生成物B为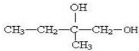 .B发生氧化反应得到C为
.B发生氧化反应得到C为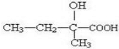 ,由C、D的分子式可知,C发生消去反应生成D,且D分子中含有2个甲基,故D为
,由C、D的分子式可知,C发生消去反应生成D,且D分子中含有2个甲基,故D为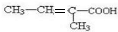 ,反应⑤属于卤代烃的水解反应,则E的结构简式为
,反应⑤属于卤代烃的水解反应,则E的结构简式为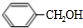 ,E和D发生酯化反应生成F为
,E和D发生酯化反应生成F为 ,据此解答.
,据此解答.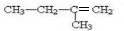 ,反应②是水解反应,生成物B为
,反应②是水解反应,生成物B为 .B发生氧化反应得到C为
.B发生氧化反应得到C为 ,由C、D的分子式可知,C发生消去反应生成D,且D分子中含有2个甲基,故D为
,由C、D的分子式可知,C发生消去反应生成D,且D分子中含有2个甲基,故D为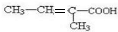 ,反应⑤属于卤代烃的水解反应,则E的结构简式为
,反应⑤属于卤代烃的水解反应,则E的结构简式为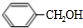 ,E和D发生酯化反应生成F为
,E和D发生酯化反应生成F为 ,
,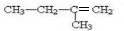 ,有4种化学环境不同的氢原子,在核磁共振氢谱中能呈现4种峰,峰面积比为3:2:3:2,故答案为:4;3:2:3:2;
,有4种化学环境不同的氢原子,在核磁共振氢谱中能呈现4种峰,峰面积比为3:2:3:2,故答案为:4;3:2:3:2; ,含有的官能团名称:羧基、羟基,故答案为:羧基、羟基;
,含有的官能团名称:羧基、羟基,故答案为:羧基、羟基; ;
; ,
, ;
; ;
; )有多种同分异构体,符合下列条件的同分异构体:①属于芳香族化合物,且含有与F相同的官能团;②苯环上有两个取代基,且苯环上的一氯代物只有两种;③其中一个取代基为-CH2COOCH3,有
)有多种同分异构体,符合下列条件的同分异构体:①属于芳香族化合物,且含有与F相同的官能团;②苯环上有两个取代基,且苯环上的一氯代物只有两种;③其中一个取代基为-CH2COOCH3,有 ,
, .
.


科目:高中化学 来源: 题型:

| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1molCO、2molH2 | 1mol CH3OH | 2molCO、4molH2 |
| CH3OH的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | 放出Q1 kJ | 吸收Q2 kJ | 放出Q3 kJ |
| 反应物转化率 | α 1 | α 2 | α 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X射线法、铜丝燃烧法、钠熔法、李比希燃烧法都是元素定性分析法 |
| B、日本福岛核电站释放的131I与137Cs,是两种不同的核素 |
| C、我国自行研制的“神七”航天服是由新型“连续纤维增韧”材料做成的,其主要成分是由碳化硅、陶瓷和碳纤维复合而成的,它是一种新型无机非金属材料 |
| D、氟氯烃是一种致冷剂,但它会破坏臭氧层,研究人员正在积极研发环保型的替代产品以减少氟氯烃的使用量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)某学习小组用0.80mol/L标准浓度的烧碱溶液测定未知浓度的盐酸.
(1)某学习小组用0.80mol/L标准浓度的烧碱溶液测定未知浓度的盐酸.| 实验编号 | 待测HCl溶液的体积(mL) | 滴入NaOH溶液的体积(mL) |
| 1 | 20.00 | 23.00 |
| 2 | 20.00 | 23.10 |
| 3 | 20.00 | 22.90 |
查看答案和解析>>
科目:高中化学 来源: 题型:

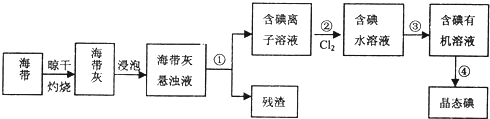
| A、加热时,①上部汇聚了固体碘,说明碘的热稳定性较差 |
| B、加热时,②、③中的溶液均变红,冷却后又都变为无色 |
| C、④中,浸泡在热水中的容器内气体颜色变深,浸泡在冰水中的容器内气体颜色变浅 |
| D、四个“封管实验”中都有可逆反应发生 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com