
| ʵ�� ��� | A��KMnO4��ҺŨ��/mol��L-1�� | B��������ҺŨ��/mol��L-1�� | C��������ҺŨ��/mol��L-1�� | ��ɫʱ��/s |
| 1 | 3 | 3 | 1 | 336 |
| 2 | 1 | 2 | 3 | 82 |
| 3 | 3 | 1 | 3 | 76 |
| 4 | 1 | 3 | 2 | 133 |
| 5 | 2 | 3 | 3 | 102 |
| 6 | 3 | 2 | 2 | 156 |
| 7 | 2 | 2 | 1 | 300 |
| 8 | 2 | 1 | 2 | 115 |
| 9 | 1 | 1 | 1 | 200 |
| | A��KMnO4��Һ�� | B��������Һ�� | C��������Һ�� | ||||||
| Ũ��/mol��L-1 | 0.005 | 0.010 | 0.015 | 0.1 | 0.5 | 0.9 | 6 | 12 | 18 |
| ƽ����ɫʱ��/s | 138.3 | 172.3 | 189.3 | 130.3 | 179.3 | 190.3 | 278.7 | 134.7 | 86.7 |
| c(H2SO4)/mol��L-1 | 18 | 16 | 14 | 12 | 10 | 8 | 6 |
| ��ɫʱ��/s | 67 | 83 | 90 | 103 | 129 | 146 | 200 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���к��Ȳⶨʵ���У�����ͭ�ʽ��������������к��ȵľ���ֵƫ�� |
| B���ô���Һ��ϴ�ζ��õ���ƿ����ʹ�ζ����ƫ�� |
| C���ζ��յ��ȡ�ζ��̶ܿ�ʱ�����ӱ�ҺҺ�棬�ᵼ�²ⶨ���ƫ�� |
| D������һ�����ʵ���Ũ�ȵ���Һ������ʱ���ӿ̶��ߣ���ʹ������ҺŨ��ƫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
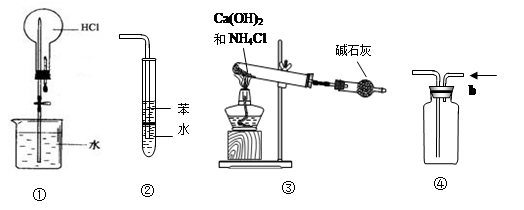
| A��װ�âٿ�������HCl��Ȫʵ�� |
| B��װ�âڿ���������HCl���壬�������� |
| C��װ�âۿ�����ʵ�����Ʊ�����NH3 |
| D��װ�â�b�ڽ������ռ�CO2������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����еμ���ˮ�Ʊ��屽 |
| B���ü�ʽ�ζ�����ȡ20.00mL KMnO4��Һ |
| C������ڵ�NaOHϡ��Һ�еμ�FeCl3������Һ�����Ʊ�Fe(OH) 3���� |
| D������I������Һ�еμ���ˮ��CCl4�������ü���I���Ĵ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����

 8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2 Na2SiO3+CO2�� Al2O3+Na2CO3
Na2SiO3+CO2�� Al2O3+Na2CO3 2NaAlO2+CO2��
2NaAlO2+CO2��| ������ | Al(OH)3 | Fe(OH)3 | Mg(OH)2 | Cr(OH)3 |
| ��ȫ����ʱ��ҺpH | 4.7 | 3.7 | 11.2 | 5.6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������ˮ�����Һ©�����ټ�����������������á����ˣ��ɴӵ�ˮ�л�ȡ�� |
| B����CuSO4��Һ�õ�CuSO4��5H2O�IJ����Ǽ���Ũ������ȴ�ᾧ �����ˡ�ϴ�ӡ����� |
| C������������з�̪��NaOH��Һ�еμ�ϡ���ᵱ��ɫǡ����ȥʱ������ҺpH=7 |
| D����ij��Һ�еμ���ˮ�μ�KSCN��Һ����Һ��죬֤����Һ�к���Fe2+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������Ͳ���϶� | B���ڵζ��ܵ��϶� |
| C����������ƽ��ߵ����� | D����������ƽ��ߵ��ұ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
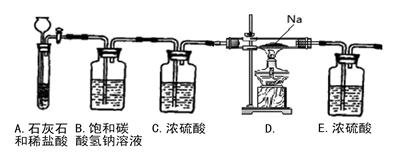
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com