
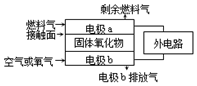
 固体氧化物燃料电池(SOFC)以固体氧化物作为电解质,其工作原理如图所示.下列关于固体燃料电池的有关说法中正确的是( )
固体氧化物燃料电池(SOFC)以固体氧化物作为电解质,其工作原理如图所示.下列关于固体燃料电池的有关说法中正确的是( )| A. | 固体氧化物的作用是让电子在电池内通过 | |
| B. | 固体氧化物中O2-从a极向b极移动 | |
| C. | 电极b为电池的负极,电极反应式为:O2+4e-=2O2- | |
| D. | 若以C3H8为燃料气,则接触面上发生的反应为C3H8-20e-+10O2-═3CO2+4H2O |
分析 A.电子不通过固体电解质;
B.阴离子向负极移动;
C.正极上氧气得电子生成氧负离子;
D.若C3H8作为燃料气,则接触面上发生的反应是C3H8失电子.
解答 解:A.固体氧化物的作用是让O2-在电池内通过,电子只能在导线和电极上移动,故A错误;
B.燃料电池中燃料在负极失电子,氧气在正极得到电子,所以a是负极,b为正极,O2-从b极向a极移动,故B错误;
C.氧气在正极得到电子,电极b为电池的正极,电极反应式为:O2+4e-=2O2-,故C错误;
D.若C3H8作为燃料气,则接触面上发生的反应是C3H8失电子,电极反应为C3H8-20e-+10O2-═3CO2+4H2O,故D正确;
故选D.
点评 本题考查了化学新型电源的原电池原理应用,主要是考查电极的书写,注意不是电解质溶液中而是固体电解质形成的原电池,侧重于考查学生的分析能力和应用能力,题目难度中等.


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:选择题
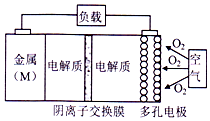 电池的“理论比能量”指单位质量的电极材料理论上能释放的最大电能.“金属(M)〜空气电池”(如下图)具有原料易得、能量密度高等优点.该类电池放电的总反应方程式为:4M+nO2+2nH2O═4M(OH) n.下列说法不正确的是( )
电池的“理论比能量”指单位质量的电极材料理论上能释放的最大电能.“金属(M)〜空气电池”(如下图)具有原料易得、能量密度高等优点.该类电池放电的总反应方程式为:4M+nO2+2nH2O═4M(OH) n.下列说法不正确的是( )| A. | “金属(M)〜空气电池”放电过程的正极反应式:O2+2H2O+4e-=4M(OH)n | |
| B. | 比较Mg、Al、Zn三种“金属-空气电池”,“Al-空气电池”的理论比能量最高 | |
| C. | 电解质溶液中的阴离子从负极区移向正极区 | |
| D. | 在“M-空气电池”中,为防止负极区沉积Mg(OH)2,宜采用中性电解质及阳离子交换膜 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
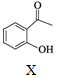 +
+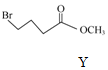 $\stackrel{HaH,DMF}{→}$
$\stackrel{HaH,DMF}{→}$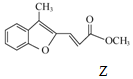 ,下列说法不正确的是( )
,下列说法不正确的是( )| A. | 物质X中所有碳原子可能共平面 | |
| B. | 可用FeCl3溶液鉴别Z中是否含有X | |
| C. | 等物质的量的X、Z分别与H2加成,最多消耗H2的物质的量之比为3:5 | |
| D. | 等物质的量的Y、Z分别与NaOH溶液反应,最多消耗NaOH的物质的量之比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 酸 | 碱 | 盐 | 混合物 | |
| A | H2SO3 | 纯碱 | 明矾 | 盐酸 |
| B | HClO4 | 熟石灰 | 石灰石 | 液氯 |
| C | HI | 烧碱 | 小苏打 | 氯水 |
| D | NaHSO4 | 一水合氨 | 食盐 | 漂白粉 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | Cl2(HCl) | NaOH溶液 |
| B | Fe2O3(Al2O3) | NaOH溶液 |
| C | Na2CO3溶液(NaCl) | AgNO3溶液 |
| D | Na2SO4溶液(Na2CO3) | 稀盐酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含ClO-的溶液中:H+、K+、Br-、I- | |
| B. | pH=1的溶液中:NH4+、Ba2+、CO32-、NO3- | |
| C. | 在与Al反应能放出H2的溶液中:Mg2+、HCO3-、SO42-、Cl- | |
| D. | 在pH=10的溶液中:Na+、K+、CH3COO-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用钠可以检验某无水酒精中是否含有水 | |
| B. | 除去甲烷中混有的少量乙烯,可以将混合气体通过酸性KMnO4溶液 | |
| C. | 制取乙酸乙酯时,试剂加入的顺序是:先加入乙醇,后慢慢加入浓硫酸,最后加入乙酸 | |
| D. | 在蔗糖溶液中加入少量稀硫酸,水浴加热后,再加入少量新制的氢氧化铜悬浊液,加热至沸腾,没有砖红色沉淀生成,说明蔗糖没有水解 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com