
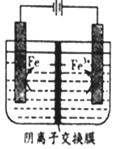
| A. | .阳极主要发生反应:Fe2+-e-═Fe3+ | |
| B. | 可用高纯铁电极作阴扱 | |
| C. | .电解液中的SO42-由右向左通过阴离子交换膜 | |
| D. | .电解法制备髙纯铁总反应:3Fe2+$\frac{\underline{\;通电\;}}{\;}$Fe+2Fe3+ |
分析 A.阳极上失电子发生氧化反应;
B.连接电源负极的为阴极,阴极材料没有特殊要求;
C.阴离子移向阳极;
D.阴极上发生Fe2++2e-═Fe,阳极上发生2Fe2+-2e-═2Fe3+,据此确定总的电极反应方程式.
解答 解:A.阳极上失电子发生氧化反应,主要发生反应为2Fe2+-2e-═2Fe3+,故A正确;
B.B.连接电源负极的为阴极,阴极材料没有特殊要求,故可用高纯铁电极作阴极,故B正确;
C.阴离子移向阳极,且连接电源正极的为阳极,故电解液中的SO42-由左向右通过阴离子交换膜,故C错误;
D.阴极上发生Fe2++2e-═Fe,阳极上发生2Fe2+-2e-═2Fe3+,总电解反应为3Fe2+$\frac{\underline{\;通电\;}}{\;}$Fe+2Fe3+,故D正确;
故选C.
点评 本题考查电解原理及应用,为高频考点,把握惰性电极及发生的电解反应为解答的关键,侧重分析与应用能力的考查,注意选项C离子移动问题,题目难度不大.


 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 只含有2个双键的直链有机物 | B. | 含1个双键的直链有机物 | ||
| C. | 含1个双键的环状有机物 | D. | 含一个三键的直链有机物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2个 | B. | 3个 | C. | 4个 | D. | 5个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | ①和②中发生的反应均为复分解反应 | |
| B. | 若将实验中的稀硫酸换成稀盐酸也能比较三种酸强弱 | |
| C. | 一段时间后②中有胶冻状物质生成 | |
| D. | 该实验能证明酸性强弱的顺序是:硫酸>碳酸>硅酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
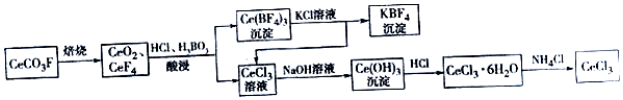
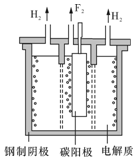
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| 实验目的 | 验证HCl水溶液的酸性 | 检验葡萄糖的醛基 | 配制一定质量分数的AlCl3水溶液 | 测定中和反应的反应热 |
| 实验方案设计 |  |  |  |  |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该电池不能用水溶液作为电解质 | |
| B. | 放电时,Li+在电解质中由负极向正极迁移 | |
| C. | 充电时,若转移1 mol e-,阴极电极将增重7g | |
| D. | 放电时,正极的电极反应式为AlLi-e-═Li++Al |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com