
| A. | Cl2→HCl | B. | NO2→HNO3 | C. | Fe2O3→Fe | D. | SiO2→H2SiO3 |
分析 A.氯气和氢气反应生成氯化氢;
B.二氧化氮和水反应生成硝酸和一氧化氮;
C.氧化铁和铝反应生成铁和氧化铝;
D,二氧化硅难溶于水不能一步反应生成硅酸.
解答 解:A.氯气和氢气反应生成氯化氢,H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl,能一步实现,故A不符合;
B.二氧化氮和水反应生成硝酸和一氧化氮,3NO2+H2O=2HNO3+NO,能一步实现,故B不符合;
C.氧化铁和铝反应生成铁和氧化铝,2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3,能一步实现,故C不符合;
D,二氧化硅难溶于水不能一步反应,需要二氧化硅和碱反应生成硅酸盐,硅酸盐和酸反应生成硅酸,故D符合;
故选D.
点评 本题考查了物质性质的综合应用,主要是氯气、二氧化氮、二氧化硅、氧化铁等物质化学性质的理解应用,题目较简单.


科目:高中化学 来源: 题型:多选题
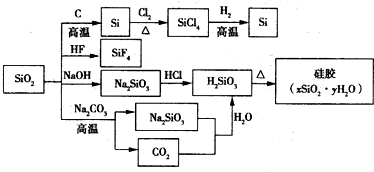
| A. | SiO2属于两性氧化物 | |
| B. | 盛放Na2CO3溶液的试剂瓶不能用玻璃塞 | |
| C. | 硅胶吸水后可重复再生 | |
| D. | 图中所示转化反应都是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
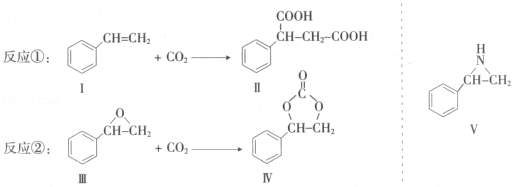
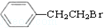 通过消去反应制备Ⅰ的化学方程式为
通过消去反应制备Ⅰ的化学方程式为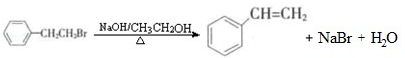 (注明反应条件).
(注明反应条件).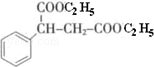 .
.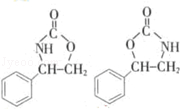 .
.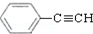 和H2三者发生反应(苯环不参与反应),生成化合物Ⅵ和Ⅶ,其分子式均为C9H8O,且都能发生银镜反应.下列关于Ⅵ和Ⅶ的说法正确的有AB(双选,填字母).
和H2三者发生反应(苯环不参与反应),生成化合物Ⅵ和Ⅶ,其分子式均为C9H8O,且都能发生银镜反应.下列关于Ⅵ和Ⅶ的说法正确的有AB(双选,填字母).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢气在氯气中燃烧产生苍白色火焰 | |
| B. | 铁丝在氯气中燃烧生成FeCl2 | |
| C. | 氯气的水溶液用于漂白,是利用氯气的强氧化性 | |
| D. | 当有大量氯气逸到空气中时,可用浸有NaOH溶液的毛巾捂住鼻子 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化剂与还原剂的物质的量之比为1:8 | |
| B. | 该过程说明Fe(NO3)2溶液不宜加酸酸化 | |
| C. | 若有1 mol NO3-发生氧化反应,则转移8 mol e- | |
| D. | Fe3+的氧化性比HNO3弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Li为电池的负极 | |
| B. | 充电时阳极反应式为:4Cl-+S+SO2-4e-═2SOCl2 | |
| C. | 电池的电解液可用LiCl水溶液代替 | |
| D. | 放电时电子从负极经外电路流向正极 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com