
| A. | 利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境 | |
| B. | 将废弃的秸秆转化为清洁高效的能源 | |
| C. | 为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术 | |
| D. | 采用新技术开采煤、石油和天然气,以满足经济发展的需要 |
科目:高中化学 来源: 题型:选择题
| A. | Na+、I-、CO32-、ClO- | B. | Ba2+、Na+、SCN-、Cl- | ||
| C. | Fe2+、H+、K+、NO3- | D. | Cu2+、Mg2+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
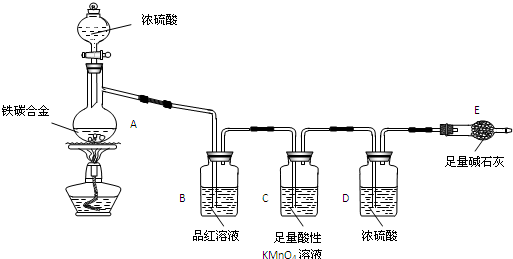
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol/L 的Na2CO3溶液中,含有的Na+离子数为2 NA | |
| B. | 0.5 mol H2SO4含有的原子数目为3.5NA | |
| C. | 32 g O2所含的分子数目为NA | |
| D. | 27g金属铝变成铝离子时失去的电子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
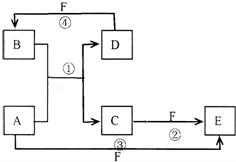 已知A、B、C、D、E、F六种物质的转化关系如图所示 (反应条件和部分产物未标出)
已知A、B、C、D、E、F六种物质的转化关系如图所示 (反应条件和部分产物未标出)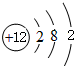 ,反应④的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.
,反应④的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 指示剂 | 变色范围 | 酸色 | 碱色 |
| 石蕊 | 5.0-8.0 | 红色 | 蓝色 |
| 酚酞 | 8.0-10.0 | 无色 | 红色 |
| 甲基橙 | 3.1-4.4 | 红色 | 黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg2+、NO3-、K+、Cl- | B. | Fe2+、NO3-、Al3+、Cl- | ||
| C. | Mg2+、SO42-、Na+、HCO3- | D. | K+、NH4+、AlO2-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
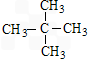 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 已知碳碳单键可以绕键轴自由旋转,分子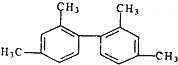 中至少有9个碳原子处于同一平面上 中至少有9个碳原子处于同一平面上 | |
| B. | 取W克乙烯和丙烯的混合气体,使之充分燃烧时,耗氧量跟混合物中各组分的质量比无关 | |
| C. | 在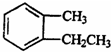 的同分异构体中,苯环上的一氯代物有两种结构的只有1种 的同分异构体中,苯环上的一氯代物有两种结构的只有1种 | |
| D. | 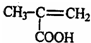 的核磁共振氢谱有3种峰,其峰面积之比为3:2:1 的核磁共振氢谱有3种峰,其峰面积之比为3:2:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com