
| A.在滴定时左手旋转酸式滴定管的玻璃活塞,右手不停地摇动锥形瓶 |
| B.两眼应时刻注视酸式滴定管内液面变化 |
| C.在滴定终点时,待指示剂变色应立即读数,否则会产生误差 |
| D.在加待测NaOH溶液时,锥形瓶应先用待测液润洗 |
科目:高中化学 来源:不详 题型:单选题
| A.不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛 |
| B.不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗 |
| C.若苯酚溶液沾到皮肤上,应立即用大量水冲洗 |
| D.配制浓硫酸和乙醇混合液时,先将浓硫注入烧杯中,然后,边加无水酒精边用玻璃棒搅拌至冷却 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 科学家研究发现,进入生物体内的氧分子,可接受1个电子转变为超氧阴离子自由基(O2-),进而引发产生一系列自由基。一切需氧生物在其机体内均有一套完整的活性氧系统(抗氧化酶和抗氧化剂),能将活性氧转变为活性较低的物质,机体因此受到保护。人们利用羟胺(NH2OH)氧化的方法可以检测其生物系统中O2-含量,原理是O2-与羟胺反应生成NO2-和一种过氧化物。NO2-在对氨基苯磺酸和α-萘胺作用下,生成粉红的偶氮染体,染体在波长530nm处有显著吸收,且其吸收值与c(NO2-)成正比,从而可计算出样品中的O2-含量。某实验室用以上方法处理后测得溶液中c(NO2-)=2.500×10-3 mol?L-1。
科学家研究发现,进入生物体内的氧分子,可接受1个电子转变为超氧阴离子自由基(O2-),进而引发产生一系列自由基。一切需氧生物在其机体内均有一套完整的活性氧系统(抗氧化酶和抗氧化剂),能将活性氧转变为活性较低的物质,机体因此受到保护。人们利用羟胺(NH2OH)氧化的方法可以检测其生物系统中O2-含量,原理是O2-与羟胺反应生成NO2-和一种过氧化物。NO2-在对氨基苯磺酸和α-萘胺作用下,生成粉红的偶氮染体,染体在波长530nm处有显著吸收,且其吸收值与c(NO2-)成正比,从而可计算出样品中的O2-含量。某实验室用以上方法处理后测得溶液中c(NO2-)=2.500×10-3 mol?L-1。| 色阶序号 | 1 | 2 | 3 | 4 | 5 | 6 |
| 加入溶液B的体积(mL) | 0 | 2.0 | 4.0 | 6.0 | 8.0 | 10.0 |
| 反应后溶液颜色 | 由无色变为由浅到深的樱桃红色 | |||||
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 混合物质量、实验前后U型管质量变化来确定混合物中氧化铜的质量分数。
混合物质量、实验前后U型管质量变化来确定混合物中氧化铜的质量分数。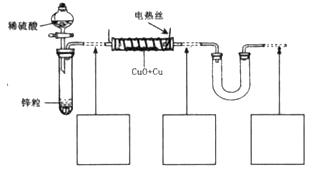
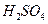 B、无水硫酸铜粉末 C、无水氯化钙颗粒
B、无水硫酸铜粉末 C、无水氯化钙颗粒
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.不慎将苯酚固体粉末沾在皮肤上,立即用大量热水(>65℃)冲洗 |
| B.在用标准盐酸滴定未知浓度NaOH溶液时,滴定前,酸式滴定管尖嘴处有气泡,而在滴定后气泡消失,会使测定结果偏低 |
| C.把玻璃管插入橡胶塞孔时,可用厚布护手,紧握用水湿润的玻管,缓慢旋进塞孔中 |
| D.银氨溶液、Cu(OH)2悬浊液、硫酸溶液、氯水在实验室里均不宜长期放置 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.某溶液中加入BaCl2溶液产生白色沉淀,加入稀硝酸后白色沉淀不溶解,说明该溶液中含有Ag+或SO42-中的至少一种 |
| B.除去AlCl3溶液中的MgCl2,可以先向溶液中加入过量NaOH溶液,过滤后向滤液中再加入适量盐酸合重新生成AlCl3 |
| C.N2中混有的少量NO2可用水洗 |
| D.NO中混有少量的H2S可用通入CuSO4溶液的方法除去 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 断滴定终点。实验步骤如下:
断滴定终点。实验步骤如下: 如果锥形瓶中含有少量蒸馏水,是否会影响测量结果 (填“是”、“否”、“不能确定”),
如果锥形瓶中含有少量蒸馏水,是否会影响测量结果 (填“是”、“否”、“不能确定”), 曲线图。
曲线图。
 、“不正确”)
、“不正确”)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在含有FeCl2杂质的FeCl3溶液中通入足量Cl2后,充分加热,除去过量的Cl2,即可得到纯净的FeCl3溶液 |
| B.向SO2溶液中分别滴加Ba(NO3)2、BaCl2、Ba(OH)2溶液,均产生BaSO3白色沉淀 |
| C.向2.0mL浓度均为0.1mol/L的KCl和Kl混合溶液中滴加1~2滴0.01 mol/LAgNO3溶液,振荡,沉淀呈黄色,说明AgCl的Ksp比AgI的Ksp大 |
| D.分别电解熔融氯化镁和熔融氯化铝可以制取金属镁和金属铝 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com