
��14�֣���1��NO2�н�ǿ�������ԣ��ܽ�SO2��������SO3����������ԭΪNO����֪��������Ӧ�����������仯��ͼ��ʾ��

��NO2����SO2���Ȼ�ѧ����ʽΪ_________________________________��
��2����2L�ܱ������з���1mol��������һ���¶Ƚ������·�Ӧ��2NH3(g) N2��g��+3H2��g����
N2��g��+3H2��g����
��Ӧʱ��(t)��������������ѹǿ(p)�����ݼ��±�
ʱ��t/min | 0 | 1 | 2 | 3 | 4 | 5 |
��ѹǿp 100 kPa | 5 | 5.6 | 6.4 | 6.8 | 7 | 7 |
��ƽ��ʱ������ת����Ϊ___________��
��3��25�棬ij��Ԫ����H2A��NaOH��Һ��Ӧ������NaHA��Na2A����Һ�к�A�����ķֲ�������ƽ��ʱij��A����Ũ��ռ����A��Ũ��֮�͵ķ���������Һ�仯���������ͼ��ʾ��
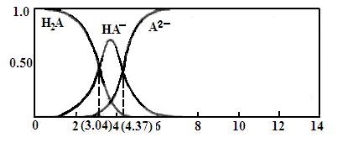
��֪��103.04��1.1��103,104.37=2.3��104 25�棬Ka1(H2CO3)= 4.4��10-7 Ka2(H2CO3) �� 4.7��10-11
������0.1NaHAmol��L-1��Һ�м�������NaOH��Һ��c(A2-)/c(HA-)��ֵ �����������С�����䡱����ͬ����c(H+)/c(OH-) ��ֵ ��
������0.1NaHAmol��L-1��Һ�м��백ˮ����Һ�����ԣ���c(H2A)+c(NH4+) c(A2-) ������ڡ�����С�ڡ����ڡ�����
�ۼ���HA����������ƽ�ⳣ��Ka2= ��
�ܽ�����H2A����Na2CO3��Һ�з�Ӧ�����ӷ���ʽΪ�� ��
��1�� NO2(g)+SO2(g)  SO3(g)+NO(g) ��H=-41.8KJ/mol�� ��2��40%��
SO3(g)+NO(g) ��H=-41.8KJ/mol�� ��2��40%��
��3������������ =���� 4.35��10-5���� 2H2A+CO32-=2HA-+CO2��+H2O
��������
�����������1������ͼһ��֪�Ȼ�ѧ����ʽΪ�� 2SO2(g) +O2(g)  2SO3(g)��H=-196.6KJ/mol; ��2NO(g)+ O2(g)
2SO3(g)��H=-196.6KJ/mol; ��2NO(g)+ O2(g)  2NO2(g) ��H=-113.0KJ/mol; �٣��������ɵ�NO2(g)+SO2(g)
2NO2(g) ��H=-113.0KJ/mol; �٣��������ɵ�NO2(g)+SO2(g)  SO3(g)+NO(g) ��H =��41.8KJ/mol����2�����ڷ�Ӧ��������̶��������н��У����Է�Ӧǰ���ѹǿ�ȵ�����������ʵ����ıȡ�2NH3(g)
SO3(g)+NO(g) ��H =��41.8KJ/mol����2�����ڷ�Ӧ��������̶��������н��У����Է�Ӧǰ���ѹǿ�ȵ�����������ʵ����ıȡ�2NH3(g)  N2��g��+3H2��g��������2xmol�İ�����Ӧ�������N2=xmol������H2=3xmol������δ��Ӧ�İ��������ʵ���Ϊ(1-2x)mol.n(ǰ)��n(��)=1����(1-2x)+x+3x��=1����1+2x��=5:7.���x=0.2.��������ת����Ϊ(2��0.2)��1��100%=40%;��3�� ������0.1NaHAmol��L-1��Һ�м�������NaOH��Һ��������Ӧ��HA-+OH-=H2O+A2-������c(A2-)/c(HA-)��ֵ�������ϼ���NaOH��Һʱ��c(H+)��С��c(OH-) ��������c(H+)/c(OH-) ��ֵ��С���ڸ��������غ�ɵ�c(Na+)= c(HA-)+ c(H2A)+ c(A2-)�����ݵ���غ�ɵã�c(Na+)+ c(H+)+ c(NH4+)= c(OH-)+ 2c(A2-)+ c(HA-)������Ϊ��Һ�����ԣ�����c(H+)= c(OH-)��������ʽ�������ɵ�c(H2A)+c(NH4+)=c(A2-)����HA-
N2��g��+3H2��g��������2xmol�İ�����Ӧ�������N2=xmol������H2=3xmol������δ��Ӧ�İ��������ʵ���Ϊ(1-2x)mol.n(ǰ)��n(��)=1����(1-2x)+x+3x��=1����1+2x��=5:7.���x=0.2.��������ת����Ϊ(2��0.2)��1��100%=40%;��3�� ������0.1NaHAmol��L-1��Һ�м�������NaOH��Һ��������Ӧ��HA-+OH-=H2O+A2-������c(A2-)/c(HA-)��ֵ�������ϼ���NaOH��Һʱ��c(H+)��С��c(OH-) ��������c(H+)/c(OH-) ��ֵ��С���ڸ��������غ�ɵ�c(Na+)= c(HA-)+ c(H2A)+ c(A2-)�����ݵ���غ�ɵã�c(Na+)+ c(H+)+ c(NH4+)= c(OH-)+ 2c(A2-)+ c(HA-)������Ϊ��Һ�����ԣ�����c(H+)= c(OH-)��������ʽ�������ɵ�c(H2A)+c(NH4+)=c(A2-)����HA- H++A2-����ͼ���֪�����ﵽ����ƽ��ʱc(HA-)=c(A2-).
H++A2-����ͼ���֪�����ﵽ����ƽ��ʱc(HA-)=c(A2-). ��������H2A���������������ĵ���ƽ�ⳣ����֪������H2A���뵽Na2CO3��Һ�з�Ӧ�����ӷ���ʽΪ��2H2A+CO32-=2HA-+CO2��+H2O��
��������H2A���������������ĵ���ƽ�ⳣ����֪������H2A���뵽Na2CO3��Һ�з�Ӧ�����ӷ���ʽΪ��2H2A+CO32-=2HA-+CO2��+H2O��
���㣺�����Ȼ�ѧ����ʽ����д�����ʵ�ת���ʵļ��㼰��Ԫ����ĵ���ƽ�ⳣ���ļ��㡢���ӷ���ʽ����д��֪ʶ��


 ��Уͨ��֤��Ч��ҵϵ�д�
��Уͨ��֤��Ч��ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ����ʮУ��һ��ѧ�����н�ѧ������⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
Ԫ�ص���������Ԫ��ԭ�������ĵ������������Ա仯��ԭ����
A��Ԫ��ԭ�ӵĺ�������Ų��������Ա仯
B��Ԫ�ص�ԭ�Ӱ뾶�������Ա仯
C��Ԫ�صĻ��ϼ۳������Ա仯
D��Ԫ�صĽ����ԡ��ǽ����Գ������Ա仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʦ���еڶ�ѧ�����п��Ը�һ��ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ʵĵݱ��У���ȷ����
A��O��Na��S��ԭ�Ӱ뾶�������� B��LiOH��KOH��CsOH�ļ���������ǿ
C��HF��NH3��SiH4���ȶ���������ǿ D��HCl��HBr��HI�Ļ�ԭ�����μ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ��ʯ���^�߶���ѧ����ͳ���Ծ��������棩 ���ͣ�ѡ����
������Һ������Ũ�ȹ�ϵ�ı�ʾ��ȷ���ǣ� ��
A��NaHCO3��Һ�У�c(H��)��c(Na��)��c(OH��)��c(CO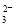 )��c(HCO
)��c(HCO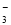 )
)
B��pH��3��CH3COOH��Һ��pH��11��NaOH��Һ�������Ϻ����Һ�У�c(OH��)>c(H��)��c(CH3COO��)
C��0.1 mol��L��1��NH4Cl��Һ�У�c(Cl��)>c(H��)>c(NH )>c(OH��)
)>c(OH��)
D�����ʵ���Ũ����ȵ�CH3COOH��CH3COONa��Һ�������Ϻ����Һ�У�
2c(Na��)��c(CH3COOH)��c(CH3COO��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ����5��ģ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ��ƶ���
��15�֣�������F�Ǻϳ�������Ѫ�ܲ�����Ҫҩ��������İ����м��塣����һ�ֺϳ�·�����£�

�ش��������⣺
��1��A�Ļ�ѧ����Ϊ �� ��2�� B����C�ķ�Ӧ����Ϊ ��
��3����C����D�Ļ�ѧ����ʽΪ�� ����4��E�ķ���ʽΪ ��
��5��F�Ľṹ��ʽΪ ��1mol F�����������Ʒ�Ӧ�����������ڱ�״���µ����Ϊ ��
��6��B�ж���ͬ���칹�壬д��ͬʱ��������������B������ͬ���칹��Ľṹ��ʽ ��
�ټ��ܷ���������Ӧ�����ܷ���ˮ�ⷴӦ��
�ں˴Ź�������ͼ��4�����շ塢�ҷ����֮��Ϊ1��2��6��3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ����5��ģ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��1L�ܱ�����������Ӧ��4NH3(g)��5O2(g) 4NO(g)��6HO(g) ��H����Q kJ�� mol��1(Q��0)�������ڲ������ʵ����ʵ���Ũ�����±���
4NO(g)��6HO(g) ��H����Q kJ�� mol��1(Q��0)�������ڲ������ʵ����ʵ���Ũ�����±���
ʱ�䣯Ũ�� | c(NH3)( mol��L-1) | c(O2)( mol��L-1) | c(NO)( mol��L-1) |
��ʼ | 0.8 | 1.6 | 0 |
��2min | 0.6 | a | 0.2 |
��4min | 0.3 | 0.975 | 0.5 |
��6min | 0.3 | 0.975 | 0.5 |
��8min | 0.7 | 1.475 | 0.1 |
��10min | 0.7 | 1.475 | 0.1 |
����˵���������
A����Ӧ�ڵ�2min����4minʱ��O2��ƽ������Ϊ0.1875 mol��L-1��min-1
B����Ӧ�ڵ�2minʱ�ı���ijһ������������������ʹ�ô����������¶�
C����4min����8minʱ�ֱ�ﵽ��ѧƽ�⣬��ƽ�ⳣ����ͬ
D���ڿ�ʼ��Ӧ��ǰ2min�ڣ��÷�Ӧ�ų�0.05QKJ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ��һ��ѧ������������ѧ�Ծ��������棩 ���ͣ������
��10�֣���ͼ�Dz��ֶ�����Ԫ�صĵ��ʼ��仯���������Һ����ת����ϵ����֪B��C��D��E�Ƿǽ������ʣ����ڳ��³�ѹ�¶������壻������G����ɫ��ӦΪ��ɫ��������I��Jͨ��״���³���̬����Ӧ���ǻ��������е�һ����Ҫ�Ĺ̵���Ӧ��

��1������E�Ľṹʽ_____________
��2��F��H2O��Ӧ�Ļ�ѧ����ʽΪ_____________________________���÷�Ӧ�б������뱻��ԭ�����ʵ����ʵ���֮����_________________
��3�����H�������ӵĵ���ʽ_______________,����H �������ӵķ�����____________________
_____________________________________________________________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�人�и������µ������ۻ�ѧ�Ծ��������棩 ���ͣ������
��15�֣�
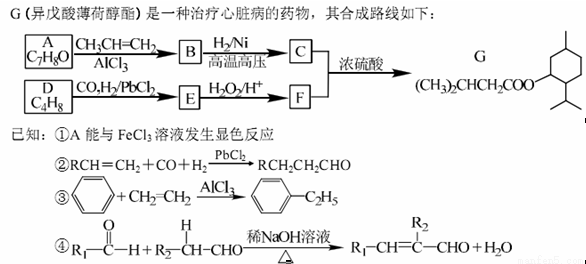
��1�� A������Ϊ�ߣߣߣ�
��2�� G�к�������������Ϊ�ߣߣߣ�
��3�� D�ķ����к��Уߣߣߣ��ֲ�ͬ��ѧ��������ԭ��
��4�� E�����Ƶ�������ͭ��Ӧ�Ļ�ѧ����ʽΪ�ߣߣߣ�
��5��д����������������A������ͬ���칹��Ľṹ��ʽ���ߣߣߣ�
A����������6��̼ԭ����һ��ֱ���ϣ�b�������к�����OH
��6�����촼���������ϡ��ٽ����ȣ�д�����Ҵ�Ϊԭ���Ʊ� �ĺϳ�·����
�ĺϳ�·����
��ͼ�����Լ����ã����ϳ�·������ʾ��ͼʾ�����£�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�˲��и���5��ģ�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ϩ�Ʒ���һ�ּ�����ҩ���ṹ��ʽ����ͼ��ʾ�������й������в���ȷ����

A����ϩ�Ʒӵķ���ʽΪC18H20O2
B����ϩ�Ʒӷ�����һ����16��̼ԭ�ӹ�ƽ��
C����ϩ�Ʒ�Ϊ�����廯����
D����ϩ�Ʒӿɷ����ӳɡ�ȡ�����������Ӿۡ�������������Ӧ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com