
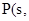 白磷
白磷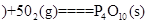 △H=-2983.2KJ/mol
△H=-2983.2KJ/mol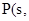 红磷
红磷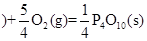 △H=-738.5KJ/mol
△H=-738.5KJ/mol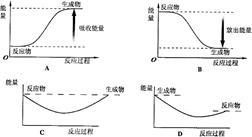
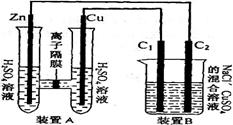
 4=
4= 

科目:高中化学 来源:不详 题型:单选题
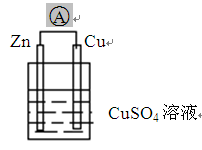
| A.X是负极,电解质溶液为CuSO4溶液 |
| B.X是负极,电解质溶液为H2SO4溶液 |
| C.X是正极,电解质溶液为CuSO4溶液 |
| D.X是正极,电解质溶液为H2SO4溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
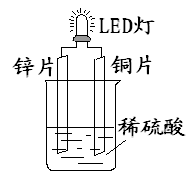
| A.铜片表面有气泡生成 |
| B.装置中存在“化学能→ 电能→ 光能”的转换 |
| C.如果将硫酸换成柠檬汁,导线中不会有电子流动 |
| D.如果将锌片换成铁片,电路中的电流方向不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.电极a是负极 |
| B.电极b上的电极反应为O2+2H2O+4e-=4OH- |
| C.外电路中电子由电极b流向电极a |
| D.氢氧燃料电池的优点是高效、对环境友好 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
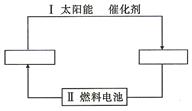
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
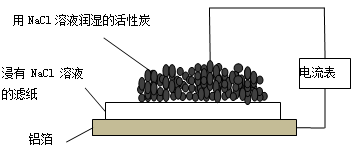
| A.该装置不能发生原电池反应 |
| B.活性炭是阴极 |
| C.总反应为:4Al+3O2 +6H2O → 4Al(OH)3 |
| D.电子从铝箔流出,经电流表、活性炭、滤纸回到铝箔 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.锌是负极,其质量逐渐减少 |
| B.氢离子在铜表面被还原,产生气泡 |
| C.电流从锌片经导线流向铜片 |
| D.电子从锌片经导线流向铜片 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com