
| A. | 14g 分子式为CnH2n的链烃中含有的C-H键的数目为2NA | |
| B. | Na2O2与H2O的反应中每生成0.1molO2,转移电子数目为0.4NA | |
| C. | 常温常压下,1.7g NH3所含电子数为0.8NA | |
| D. | 标准状况下,11.2L NO与11.2LO2混合,原子总数小于2NA |
分析 A、CnH2n的最简式为CH2;
B、过氧化钠和水反应生成氧气时,氧元素的价态由-1价变为0价;
C、求出氨气的物质的量,然后根据氨气中含10个电子来分析;
D、NO和氧气反应后生成二氧化氮,但此过程中原子个数一定守恒.
解答 解:A、CnH2n的最简式为CH2,故14gCnH2n中含有的CH2的物质的量为1mol,故含2NA条C-H键,故A正确;
B、过氧化钠和水反应生成氧气时,氧元素的价态由-1价变为0价,故当生成0.1mol氧气时反应转移0.2NA个电子,故B错误;
C、1.7g氨气的物质的量为0.1mol,而氨气中含10个电子,故0.1mol氨气中含NA个电子,故C错误;
D、NO和氧气反应后生成二氧化氮,但此过程中原子个数一定守恒,故反应后的其中的原子个数与标准状况下,11.2L NO与11.2LO2中的原子个数相同.而标准状况下,11.2L NO与11.2LO2的物质的量均为0.5mol,且两者均为双原子分子,故0.5molNO和0.5mol氧气的混合气体中含有原子的物质的量为2mol,个数为2NA个,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意公式的运用和物质的结构特点.


 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 干电池中Zn为正极,碳为负极 | |
| B. | 干电池可以实现化学能向电能的转化和电能向化学能的转化 | |
| C. | 干电池长时间连续使用时内装糊状物可能流出腐蚀电器 | |
| D. | 干电池工作时,电子由碳极经外电路流向Zn极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 常温下,向0.l mol.L-lNa2A溶液中,不断通入HC1,H2A、HA-、A2-在溶液中所占物质的量分数(δ)与pOH[pOH=-lgc(OH-)]的关系如图所示,下列说法正确的是( )
常温下,向0.l mol.L-lNa2A溶液中,不断通入HC1,H2A、HA-、A2-在溶液中所占物质的量分数(δ)与pOH[pOH=-lgc(OH-)]的关系如图所示,下列说法正确的是( )| A. | H2A的第二级电离平衡常数为l0-l0mol/L | |
| B. | 随着HCl的通入,$\frac{c({H}^{+})}{c({H}_{2}A)}$先减小后增大 | |
| C. | 当溶液呈中性时:c(Na+)═c(HA-)+2c (A2-) | |
| D. | 将等浓度等体积的Na2A与H2A溶液混合后,溶液显碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol HNO3见光分解,转移的电子数为4NA | |
| B. | 25℃时,1LpH=1的H2SO4溶液中含有的H+数为0.1NA | |
| C. | 28 g乙烯与丙烯的混合物中含有的共用电子对数为6NA | |
| D. | 将0.5molNH4NO3溶于稀氨水中使溶液呈中性,溶液中NH4+的数目为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 富脂食品包装中常放入活性铁粉袋,以防止油脂氧化变质 | |
| B. | 目前科学家已经制得单原子层锗,其电子迁移率是硅的10倍,有望取代硅用于制造晶体管 | |
| C. | Ni-Zn化合物的纳米颗粒可作 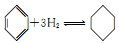 反应的催化剂,提高苯的转化率 反应的催化剂,提高苯的转化率 | |
| D. | 用K2FeO4代替Cl2处理饮用水时,既有杀菌消毒作用,又有净水作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷是正四面体结构,性质活泼,常温下能与强酸、强碱发生剧烈反应 | |
| B. | 乙烯是通过石油裂解得到的,属于不饱和烃 | |
| C. | 苯与氢气、液溴、浓硝酸的反应类型相同 | |
| D. | 乙酸又名醋酸,其官能团是醚基,可以与乙醇发生反应生成乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
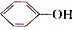 )具有弱酸性,其Ka=1.1×10-l0;水杨酸第一级电离形成的离子
)具有弱酸性,其Ka=1.1×10-l0;水杨酸第一级电离形成的离子 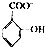 能形成分子内氢键.据此判断,相同温度下电离平衡常数Ka2(水杨酸)<Ka(苯酚)(填“>”或“<”),其原因是
能形成分子内氢键.据此判断,相同温度下电离平衡常数Ka2(水杨酸)<Ka(苯酚)(填“>”或“<”),其原因是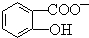 中形成分子内氢键,使其更难电离出H+,故Ka2<Ka.
中形成分子内氢键,使其更难电离出H+,故Ka2<Ka.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3.4g H2O2中含有的共用电子对数为0.1NA | |
| B. | 25℃,pH=13的NaOH溶液中,含有OH-的数目为0.1NA | |
| C. | 标准状况下,11.2 L由CH4和C2H4组成的混合气体中含有氢原子的数目为2NA | |
| D. | 标准状况下,2.24L氯气溶于水发生反应,转移的电子数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为了防止富脂食品氧化变质,延长食品的保质期,常在包装袋中放入生石灰 | |
| B. | 海水中含有丰富的碘元素,因此碘被称为“海洋元素” | |
| C. | 工业生产玻璃、水泥、漂白粉,均需要用石灰石为原料 | |
| D. | 可以利用氯化铁溶液的酸性清除铜镜表面的铜锈 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com