
【题目】已知某化学反应A2(g)+2B2(g)=2AB2(g)(AB2的分子结构为B—A—B)的能量变化如图所示,下列有关叙述中正确的是( )
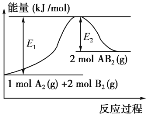
A.该反应的进行一定需要加热
B.该反应的ΔH=-(E1-E2)kJ/mol
C.该反应为吸热反应
D.断裂1molA—A键和2molB—B键放出E1kJ能量
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )。
A.在一定条件下,等物质的量的乙烯和苯分别和足量氢气发生加成反应,消耗氢气的物质的量之比为![]()
B.与甲烷、乙烯相比,苯的独特性质具体来说是易取代,能加成,难氧化
C.除去乙烷中混有的乙烯,应在一定条件下通入氢气,使乙烯转化为乙烷
D.某有机物的结构简式为![]() ,其分子结构中处在同平面内的原子最多有15个
,其分子结构中处在同平面内的原子最多有15个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种短周期元素分别位于三个周期,它们的原子序数依次增大。A与D同主族,B与E同主族,C与F同主族。且C与F能形成原子个数比为2∶1的化合物M和原子个数比为3:1的化合物N。已知E元素为地壳中含量居第2位的元素,D为金属。
(1)写出下列元素符号:A__________,B__________,C__________,D__________,E__________,F__________。
(2)M能在一定条件下生成N,写出反应的化学方程式:__________。
(3)写出F在元素周期表中的位置:__________。
(4)写出工业上用B来制备单质E的化学方程式:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应C(s)+H2O(g)![]() CO(g)+ H2(g) 在一可变容积的密闭容器中进行,在其它条件不变的情况下,下列条件的改变对其反应速率几乎无影响的是 ( )
CO(g)+ H2(g) 在一可变容积的密闭容器中进行,在其它条件不变的情况下,下列条件的改变对其反应速率几乎无影响的是 ( )
A.增加H2O的物质的量浓度B.将容器的体积缩小一半
C.保持体积不变,充入N2使体系压强增大D.保持压强不变,充入N2使容器体积变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表中七个周期可填充的元素种类如下表所示:
周期数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
元素种类 | 2 | 8 | 8 | 18 | 18 | 32 | 32 |
(1)第6、7周期均比第4、5周期多了14种元素,其原因是__。
(2)周期表中__族所含元素最多。
(3)请分析周期数与元素种类的关系,可推测出第8周期可能含有的元素种类为__(填序号)。
A.18 B.32 C.50 D.64
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物Z是合成平喘药沙丁胺醇的中间体,可通过下列路线制得:

下列说法正确的是
A.X、Y、Z均属于芳香烃B.X分子中所有原子在同一平面上
C.可用FeCl3溶液鉴别Y和ZD.1 mol Z最多能与2 mol NaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用分类的方法和氧化还原反应的规律,能实现某些物质的转化。
(1)请从下列试剂中选择合适的试剂完成指定转化(试剂可以重复选择)。
试剂:Cl2、HCl、Na2S、H2O;
①I2→IO3-的离子方程式:____;
②CuSO4→Na2SO4的化学方程式:_____。
(2)利用水钴矿(主要成分是Co2O3,含少量Fe2O3、Al2O3)制取CoC2O4·2H2O的流程如下:

①“还原”时,Fe3+和Co3+均被还原为正二价阳离子,写出Co3+被还原的离子方程式_。
②“氧化”反应的离子方程式为:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮族元素在化学领域具有重要的地位。请回答下列问题:
(1)基态氮原子的价电子轨道表示式为___________;第二周期的元素中,第一电离能介于B和N之间的元素有___________种。
(2)雌黄的分子式为As2S3,其分子结构如图所示:![]() As原子的杂化类型为___________。
As原子的杂化类型为___________。
(3)①向CuSO4溶液中加入少量氨水生成蓝色沉淀,继续加入氨水沉淀溶解,得到深蓝色透明溶液,向该溶液中加入一定量的乙醇,析出[Cu(NH3)4]SO4·H2O固体。SO42-的空间构型为___________;[Cu(NH3)4]SO4·H2O固体中含有的化学键有___________(填标号)。
A.离子键 B.共价键 C.氢键 D.金属键 E.配位键
若要确定[Cu(NH3)4]SO4·H2O是晶体还是非晶体,最科学的方法是进行___________实验。
②已知NF3与NH3分子的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,原因是___________。
(4)大π键可用![]() 表示,其中n、m分别代表参与形成大π键的原子个数和电子数,如苯分子中大π键表示为
表示,其中n、m分别代表参与形成大π键的原子个数和电子数,如苯分子中大π键表示为![]() 。N2O分子中的大π键表示为_________________。
。N2O分子中的大π键表示为_________________。
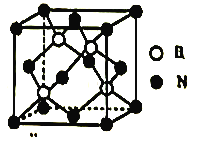
(5)立方氮化硼晶胞如图,其密度为ρg/cm3,氮化硼的摩尔质量为Mg/mol,阿伏加德罗常数的值为NA,硼原子的半径为r cm,则硼原子的空间占有率为____________________(用含有ρ、M、NA、r的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2020年5月1日起,新版《北京市生活垃圾管理条例》正式实施,下列垃圾分类对应不正确的是
|
|
|
|
A. 鸡蛋壳、剩饭菜 | B. 市民使用后一次性口罩 | C. 过期药品 | D. 一 次性干电池 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com