
相同温度下,体积均为0.25 L的两个恒容密闭容器中发生可逆反应:
X2(g)+3Y2(g)  2XY3(g) ΔH=—92.6KJ/mol
2XY3(g) ΔH=—92.6KJ/mol
实验测得反应在起始、达到平衡时的有关数据如下表所示:

下列叙述不正确的是
A.容器①、②中反应的平衡常数相等
B.达平衡时,两个容器中XY3的物质的量浓度均为2 mol/L
C.容器②中反应达到平衡时放出的热量为Q
D.若将容器①体积缩小为0.20 L,则达平衡时放出的热量大于23.15 kJ
C
【解析】
试题分析:由于反应是在相同温度下进行的,所以反应达到平衡时容器①、②中反应的平衡常数相等,正确;B.在相同温度下反应在容积相等的容器内进行。对于②来说,假设0.8mol的XY3是消耗X2、Y2反应产生的,则反应开始时X2、Y2的物质的量是1.0mol、3.0mol,与①相同,由于加入1mol的X2、3mol的Y2反应达到平衡时放出热量是23.15KJ,则反应消耗的X2的物质的量是23.15KJ÷ 92.6KJ/mol =0.25mol,则达到平衡时产生XY3的物质的量是0.50mol,其平衡浓度均为0.50mol÷0.25L=2 mol/L,正确;C.容器①、②的平衡状态等效。正反应是放热反应,逆反应是吸热反应,由于容器②中开始加入了0.8mol的 XY3,所以反应达到平衡时放出的热量小于23.15KJ,即小于Q,错误;D.若将容器①体积缩小为0.20 L,由于减小体积,也就增大的图像的压强,增大压强,平衡向气体体积减小的正反应方向移动,所以达平衡时放出的热量大于23.15 kJ,正确。
考点:考查可逆反应平衡状态的判断、物质的平衡浓度、反应热的多少及平衡常数大小比较的知识。


科目:高中化学 来源:2014-2015学年福建省高三上学期第四次月考化学试卷(解析版) 题型:选择题
中学常见物质A、B、C、D、E、X,存在转化关系 (部分生成物和反应条件略去):
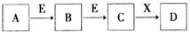 。下列推断不正确的是
。下列推断不正确的是
A.若D是一种白色沉淀,在空气中最终变为红褐色,则A可能是铁
B.若D是一种强碱,则A、B、C均可与X反应生成D
C.若D为NaCl,且A可与C反应生成B,则E可能是CO2
D.若D是一种强酸,则A既可以是单质,也可以是化合物,且D可与铜反应生成B或C
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高三上学期10月月考化学试卷(解析版) 题型:选择题
有下列符号:35Cl和37Cl、O2和O3、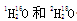 。下列有关说法正确的是
。下列有关说法正确的是
A.35和37表示的是质量数 B.35Cl和37Cl互称为同素异形体
C.O2和O3是氧元素的两种同位素 D.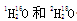 的相对分子质量相同
的相对分子质量相同
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省德阳市高三一诊考试化学试卷(解析版) 题型:选择题
X、Y、Z、W为四种短周期主族元素,它们在周期表中的位置如右图所示。X的最高价氧化物和气态氢化物的分子都是由极性键形成的非极性分子。下列性质比较中正确的是

A.最高价氧化物的水化物的酸性:Y<X<W
B.离子半径由小到大的顺序:W<Z<Y
C.单质晶体的熔点由低到高的顺序:Y<W<Z
D.原子最外层的电子数:Z<Y<X
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省德阳市高三一诊考试化学试卷(解析版) 题型:选择题
下列过程没有发生化学反应的是
A.用氢氟酸来刻蚀玻璃器皿 B.用活性炭去除冰箱中的异味
C.用煤液化和气化得到清洁燃料 D.用热碱溶液清除炊具上残留的油污
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省日照市高三12月校际联合检测化学试卷(解析版) 题型:选择题
向密闭容器中充入物质A和B,发生反应aA(g)+bB(g)  cC(g)。反应过程中,物质A的含量(A%)和C的含量(C%)随温度(T)的变化曲线如图所示,下列说法正确的是
cC(g)。反应过程中,物质A的含量(A%)和C的含量(C%)随温度(T)的变化曲线如图所示,下列说法正确的是
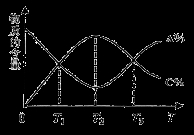
A.该反应在T1、T3温度时达到过化学平衡
B.该反应在T2温度时达到过化学平衡
C.该反应的逆反应是放热反应
D.升高温度,平衡会向正反应方向移动
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省日照市高三12月校际联合检测化学试卷(解析版) 题型:选择题
下列有关常见金属和非金属及其化合物的说法正确的是
A.Na、Al、Fe、Cu都能导电,它们的氧化物都能与酸反应
B.CO2、NO、SO2都是非金属氧化物,都属于酸性氧化物
C.铝热反应是指铝能将所有的金属从其氧化物中置换出来
D.CaCO3+SiO2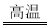 CaSiO3+CO2↑的发生,说明硅酸的酸性强于碳酸
CaSiO3+CO2↑的发生,说明硅酸的酸性强于碳酸
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省英文学校高三上学期12月月考化学试卷(解析版) 题型:填空题
(9分)氮及其化合物在很多方面有重要的用途。
(1)氮的氧化物有多种。现有NO和NO2的混合气体,其中N 、O元素质量之比为7:12,则该混合气中NO和NO2的物质的量之比为 。
(2)氨气的实验室制法有多种,若不加热,制取氨气所用试剂可以用浓氨水和生石灰,产生氨气的原因是: ;氨气的检验方法是: 。
(3)硝酸具有很强的氧化性,王水是浓硝酸与浓盐酸的混合液,可以溶解金、铂等金属。铂溶于王水时产生[PtCl6]2-和一种无色气体,该气体遇空气变为红棕色,写出该反应的离子方程式 。
(4)氮的一种氢化物肼(即N2H4)用作发射卫星的燃料。
已知: N2 + 2O2 = 2NO2 N2H4 + O2 = N2 + 2H2O
发射卫星用气体肼为原料,以NO2为氧化剂,两种物质反应生成氮气和水蒸气,反应中每有4mol电子转移,则生成N2质量为 g。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高三上学期12月月考化学试卷(解析版) 题型:选择题
已知298K时,2SO2(g)+O2(g) 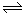 2SO3(g) △H=-197kJ/mol。在相同温度下,向密闭容器通入2mol SO2和1mol O2达平衡时,放热Q1;向另一相同体积的密闭容器中通入1mol SO2和0.5mol O2达平衡时,放出热量Q2,则下列关系式正确的是
2SO3(g) △H=-197kJ/mol。在相同温度下,向密闭容器通入2mol SO2和1mol O2达平衡时,放热Q1;向另一相同体积的密闭容器中通入1mol SO2和0.5mol O2达平衡时,放出热量Q2,则下列关系式正确的是
A.Q1=Q2/2 B.Q2<Q1<197kJ
C.Q2=Q1<197kJ D.以上均不正确
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com