
【题目】I.(1)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜。写出反应的离子方程式:_______________________。
(2)控制其他条件相同,印刷电路板的金属粉末用10%H2O2和3.0 mol/L的H2SO4混合溶液处理,测得不同温度下铜的平均溶解速率(见下表)。
温 度(T) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
铜平均溶解速率×10-3mol·L-1·min-1 | 7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
当温度高于40℃时,铜的平均溶解速率随着反应温度升高而下降,其主要原因是________________________________________________。
(3)在提纯后的CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl沉淀,制备CuCl的离子方程式是_________________________________________。
II.生活污水中的磷和氮主要以磷酸盐和铵盐形式存在。
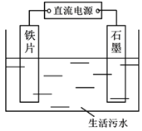
(1)除磷的原理如上图所示,利用电解法将PO43-转化为Fe3(PO4)2沉淀除去。铁作___________,(填“阴极”“阳极”),用化学用语表示产生Fe2+的主要过程:__________________________。
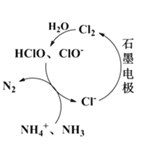
(2)有Cl-存在时,除氮原理如图所示,主要依靠电解产生的有效氯(HClO、ClO-)将NH4+或NH3氧化为N2.当pH<7时,主要发生HClO氧化NH4+的反应,其离子方程式为:_________________________________。
【答案】Cu+H2O2+2H+=Cu2++2H2O H2O2分解速率加快 2Cu2++SO32-+2Cl-+H2O![]() 2CuCl↓+SO42-+2H+ 阳极 Fe-2e-=Fe2+ 3HClO+2NH4+=3Cl-+N2↑+3H2O+5H+
2CuCl↓+SO42-+2H+ 阳极 Fe-2e-=Fe2+ 3HClO+2NH4+=3Cl-+N2↑+3H2O+5H+
【解析】
I.(1)由题可知,H2O2作为氧化剂,故其还原产物为H2O,Cu作为还原剂,氧化产物为Cu2+,H2O2中O元素化合价从-1降低为-2,化合价降低1,Cu元素化合价升高2,根据转移电子守恒、电荷守恒、原子守恒可配平其离子反应方程式为:Cu+H2O2+2H+=Cu2++2H2O;
(2)双氧水不稳定,温度高易分解,温度高于40℃时,双氧水分解速率加快,氧化铜的浓度就降低,所以铜的平均溶解速率随着反应温度升高而下降;
故答案为:H2O2分解速率加快;
(3)由题可知,该反应中CuSO4反应后化合价降低1价,故Na2SO3中S化合价升高,其生成物为Na2SO4,根据转移电子守恒、电荷守恒、原子守恒可配平其离子反应方程式为:2Cu2++SO32-+2Cl-+H2O![]() 2CuCl↓+SO42-+2H+;
2CuCl↓+SO42-+2H+;
II.(1)利用电解法将PO43-转化为Fe3(PO4)2沉淀除去,故溶液中需要Fe2+,因此铁作阳极;其在阳极上失去电子,其电极反应式为:Fe-2e-=Fe2+;
(2)由题可知,HClO发生反应后被还原为Cl-,Cl化合价降低2价,NH4+被氧化为N2,化合价升高3价,根据化合价升降守恒可知,HClO与NH4+的系数比为3:2,然后根据电荷守恒、原子守恒以及溶液呈酸性可配平其离子反应方程式为:3HClO+2NH4+=3Cl-+N2↑+3H2O+5H+。


科目:高中化学 来源: 题型:
【题目】根据反应:Zn+2H+=H2↑+Zn2+,设计如图所示原电池,观察到Y电极上有气泡产生,下列说法错误的是( )
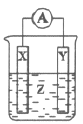
A.Y电极可能是铜
B.Z可能是硫酸铜溶液
C.电子流动方向:X→导线→Y
D.X电极的反应式:Zn-2e-=Zn2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境问题已成为人类共同关注的话题,燃煤废气、汽车尾气中常含有的NOx、SO2、H2S等污染物,容易形成酸雨,破坏环境。其综合治理是当前重要的研究课题。
Ⅰ.以下是对酸雨的若干项评价,其中不正确的是__________
a.杀死水中的浮游生物,减少鱼类食物的来源,破坏水生生态系统
b.对电线、铁轨、桥梁、房屋等均会造成严重损害
c.导致臭氧层空洞
d.二氧化碳的过量排放,是形成酸雨的主要原因之一
Ⅱ.电解法处理氮氧化物废气有较高的环境效益和经济效益(图中电极均为石墨)。

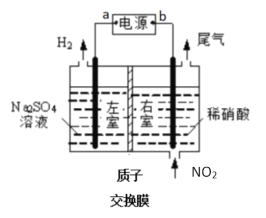
(1)电解NO制备NH4NO3原理如上方左图所示:
①阳极为石墨_____(填1或2),该电极的反应式为_____________。
②为使电解的副产物也完全转化为NH4NO3,需要补充的物质X的化学式为___________。
(2)用上方右图装置进行模拟电解NO2气体实验,可回收硝酸。
①外接电源a极为______极,左室发生的电极反应式为_____________。
②若有标准状况下2.24L NO2被吸收,通过质子交换膜(只允许质子通过)的H+为______mol。
③用含NO和NO2(不考虑NO2转化为N2O4)的废气进行模拟电解法吸收实验。电解过程中,有部分NO转化为HNO2。实验结束时,测得右室溶液中增加了1 mol HNO3、0.1 mol HNO2,同时左室收集到标准状况下28L H2。原气体中NO和NO2的体积比为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酰紫草素具有抗菌、抗炎、抗病毒、抗肿瘤等作用,它的结构简式如图所示,下列有关乙酰紫草素的说法正确的是

A. 该分子中含有1个手性碳原子
B. 1mol乙酰紫草素最多可与2mol NaOH反应
C. 1mol 乙酰紫草素最多可与2mol Br2反应
D. 能与FeCl3溶液发生显色反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO还原脱硝技术可有效降低烟气中的NOx的排放量。
(1)汽车在行驶过程中会产生有害气体CO、NO,在催化剂作用下发生如下脱硝反应:![]() ,该反应平衡常数的表达式K=______________,在570 K时,K值极大,为1×1059,但汽车上仍需装备尾气处理装置,其可能原因是________________。
,该反应平衡常数的表达式K=______________,在570 K时,K值极大,为1×1059,但汽车上仍需装备尾气处理装置,其可能原因是________________。
(2)以Mn3O4 为脱硝反应的催化剂,研究者提出如下反应历程,将历程补充完整。
第一步:___________________________________;
第二步:![]()
(3)T℃、2L密闭容器中,充入各1mol的CO和NO混合气体,加入Mn3O4发生脱硝反应,t0 时达到平衡,测得反应过程中CO2的体积分数与时间的关系如下图所示:
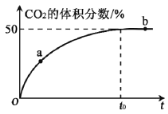
①比较大小:a处v正______b处v逆(填“>”、“<”或“=”)
②若t0 =10min,反应从开始到达平衡CO气体的平均反应速率v( CO) =_____。
③NO的平衡转化率为______,T℃时反应的化学平衡常数K=_________。
④T℃时,某时刻测得体系中各物质的量如下:n(CO)=0.2mol,n(NO)=0.2mol,n(N2)=0.1mol,n(CO2)=0.2mol,则此时该反应_______进行(填“向正反应方向”“向逆反应方向”或“处于平衡状态”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
A.放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2
B.充电时阳极反应为:Fe(OH)3-3e-+5OH-=FeO42-+4H2O
C.充电时,蓄电池的负极应与外接电源正极相连
D.放电时负极附近溶液的碱性减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝土矿的主要成分是Al2O33H2O,还含有SiO2、Fe2O3等杂质。工业上从铝土矿中提取Al可采用如图所示工艺流程。(部分操作名称及反应条件已略去)

(1)B是___,X是___,若将盐酸与X互换,则B是___。
(2)生成C的离子方程式是___。
(3)D中的溶质是___,通入CO2后生成F的化学方程式是___,F的一种用途是___。
(4)由M生成铝的化学方程式是___,当有5.4g铝生成时,转移电子___mol。
(5)上述流程中的CO2能否用盐酸代替?理由是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸工业的重要反应之一:2SO2(g)+O2(g)![]() 2SO3(g)下列叙述不正确的是( )
2SO3(g)下列叙述不正确的是( )
A.其他条件不变,升高温度可增大SO3的生成速率
B.使用合适的催化剂,是为了增大化学反应速率
C.该反应达到化学平衡状态时,SO2可100%转化为SO3
D.该反应达到化学平衡状态时,SO3的浓度不再改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.水是极弱的电解质,它能微弱电离生成相同物质的量的H+和OH-
B.稀溶液中c(H+)c(OH-)=KW,任何条件下KW都保持不变
C.无论在什么条件下,中性溶液的c(H+)一定等于1×10-7mol/L
D.H2O![]() H++OH-是一吸热反应,所以温度升高,KW也随之减小
H++OH-是一吸热反应,所以温度升高,KW也随之减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com