
| A. | 氖元素的相对原子质量是a | |
| B. | 该氖原子的摩尔质量是aNAg | |
| C. | Wg该氖原子的物质的量一定是$\frac{W}{{a{N_A}}}$mol | |
| D. | Wg该氖气的体积是22.4$\frac{W}{{a{N_A}}}$升 |
分析 某氖原子一个原子质量是a g,该氖原子的摩尔质量为aNA g/mol,其相对原子质量为aNA,根据n=$\frac{m}{M}$计算出Wg该氖原子的物质的量;不是标准状况下,不能根据标况下的气体摩尔体积计算气体体积,据此进行解答.
解答 解:A.某氖原子一个原子质量是a g,该氖原子的摩尔质量为aNA g/mol,其相对原子质量为aNA,故A错误;
B.摩尔质量的单位为g/mol,该氖原子的摩尔质量为aNA g/mol,故B错误;
C.Wg该氖原子的物质的量为:$\frac{Wg}{a{N}_{A}g/mol}$=$\frac{W}{{a{N_A}}}$mol,故C正确;
D.不是标况下,不能使用标况下的气体摩尔体积计算,故D错误;
故选C.
点评 本题考查物质的量的计算与判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确标况下气体摩尔体积的使用条件,试题有利于提高学生灵活运用基础知识解决实际问题的能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 石油裂化主要得到乙烯 | |
| B. | 石油分馏在分馏塔中进行,是化学变化,可得到汽油、煤油 | |
| C. | 煤干馏主要得到焦炭、煤焦油、粗氨水和焦炉气等 | |
| D. | 煤制煤气是物理变化,是高效、清洁地利用煤的重要途径 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 卤制品中可添加亚硝酸盐作为增色剂 | |
| B. | 补血剂口服液中添加的维生素C作为氧化剂 | |
| C. | 中国古代用明矾溶液做铜镜表面铜锈的除锈剂 | |
| D. | 月饼包装盒内放有小袋铁粉主要作为干燥剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
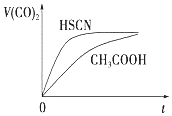 已知 25℃时部分弱电解质的电离平衡常数数据如表:
已知 25℃时部分弱电解质的电离平衡常数数据如表:| 化学式 | HSCN | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.3×10-1 | 1.8×10-5 | Ka1=4.3×10-1Ka2=5.6×10-1 | 3.0×10-8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用50mL量筒量取2.35mL稀硫酸 | |
| B. | 用托盘天平称5.56gKCl固体 | |
| C. | 配制100mlL浓度为1 mol/L的食盐水需称食盐5.9g | |
| D. | 用酒精可以萃取碘水中的碘 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 30% | B. | 10% | C. | 20% | D. | 24% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该饱和溶液硫酸铜物质的量浓度为c=$\frac{4a}{v}$ mol•L-1 | |
| B. | 该饱和溶液中硫酸铜的质量分数为w=$\frac{16a}{a+b}$% | |
| C. | 25℃硫酸铜的溶解度为 S=$\frac{1600a}{9a+25b}$g | |
| D. | 该饱和硫酸铜溶液的密度为ρ=$\frac{a+b}{v}$g•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验目的 | 实验操作 | |
| A | 比较水和乙醇中氢的活泼性 | 分别讲少量钠投入到盛有水和乙醇的烧杯中 |
| B | 由MgCl2溶液制备无水MgCl2 | 将MgCl2溶液加热蒸干 |
| C | 除去Cu粉中混有的CuO | 加入稀硝酸溶液,过滤、洗涤、干燥 |
| D | 制备Fe(OH)3胶体 | 将NaOH浓溶液滴加到饱和的FeCl3溶液中 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化铁溶液与铜反应:Fe3++Cu═Fe2++Cu2+ | |
| B. | 硅酸钠与稀硫酸反应:Na2SiO3+2H+═2Na++H2SiO3↓ | |
| C. | 氯气与水反应:Cl2+H2O═2H++Cl-+ClO- | |
| D. | 氢氧化镁与稀盐酸反应:Mg(OH)2+2H+═Mg2++2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com