
����Ŀ���ҹ���������Դ�����ܷḻ�������Դ�������Ҫ�ɷ�Fe3O4���ͳ�������Ҫ�ɷ���Fe2O3�����ֿ�ʯΪ����ij���ֳ�����ij�ֿ�ʯ������ԭ�ϣ���Ҫ�����ֿ�ʯ��Ʒ������̽����ʯ�����ļ�̬�Ͳⶨ��Ԫ�صĺ���������һЩʵ�飮 I�������ʯ��Ʒ���Ƿ���Fe2+��Fe3+
ʵ��������裺
��1�����˲������õ��IJ��������� ��
��2��������Fe2+��Fe3+���õĻ�ѧ�Լ��У�KSCN��Һ��������ˮ��KMnO4��Һ��H2O2��Һ�� �ټ���Fe3+ѡ ��
�����ʵ�鷽����֤������Һ�м���Fe2+����Fe3+ ��
��3��II���ⶨ��ʯ����Ԫ�صĺ��� ������ʵ���г�ȡ28g��ʯ��Ʒ���������ܡ����˺�õ�200ml��Һ����ȡ��20ml��Һװ����ƿ�У�������ƿ�м��������ữ��SnCl2��Һ����ַ�Ӧ���ټ���HgCl2��ȥ������SnCl2 �� ������20ml0.25mol/L��K2Cr2O7��Һǡ����ȫ��Ӧ����������Ҫ��Ӧ���£�2FeCl3+SnCl2=2FeCl2+SnCl4��6Fe2++Cr2O72��+14H+=6Fe3++2Cr3++7H2O�������ʯ��Ʒ����Ԫ�ص����������� ��
���𰸡�
��1������������ͨ©�����ձ�
��2��KSCN��Һ��ȡ������Һ�ֱ������֧�Թ���,��һ֧�Թ��е�������KMnO4��Һ,��KMnO4��Һ��ɫ,˵����Fe2+��������һ֧�Թ��е���KSCN��Һ,��Һ���,˵����Fe3+
��3��60%
�����������⣺I����1�����˲������õ��IJ��������в���������ͨ©�����ձ���
���Դ��ǣ�����������ͨ©�����ձ�����2���ټ���Fe3+ѡKSCN��Һ������������KSCN��Һ��Ѫ��ɫ��
���Դ��ǣ�KSCN��Һ��
��֤������Һ�м���Fe2+����Fe3+���������Ӽ�����Ҫ�����仹ԭ�ԣ�ѡ����������Һ�������Ӽ���ѡ��KSCN��Һ���飬���������Ϊ��ȡ������Һ�ֱ������֧�Թ��У���һ֧�Թ��е�������KMnO4��Һ����KMnO4��Һ��ɫ��˵����Fe3+��������һ֧�Թ��е���KSCN��Һ����Һ��죬˵����Fe3+��
���Դ��ǣ�ȡ������Һ�ֱ������֧�Թ��У���һ֧�Թ��е�������KMnO4��Һ����KMnO4��Һ��ɫ��˵����Fe3+��������һ֧�Թ��е���KSCN��Һ����Һ��죬˵����Fe3+��
II����3��2FeCl3+SnCl2=2FeCl2+SnCl4��6Fe2++Cr2O72��+14H+=6Fe3++2Cr3++7H2O��
�õ�
6FeCl3��6FeCl2��6Fe2+�� | Cr2O72�� |
6 | 1 |
n | 0.0 20L��0.25mol/L |
n=0.0 20L��0.25mol/L��6=0.03mol
200ml��Һ����Ԫ�����ʵ���=0.03mol�� ![]() =0.3mol��
=0.3mol��
��ʯ��Ʒ����Ԫ�ص���������= ![]() ��100%=60%��
��100%=60%��
���Դ��ǣ�60%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڽ����˵������ȷ����(����)
A. ������۲�����
B. �������Ӳ���ͨ����ֽ
C. ������������ͣ�ġ���������˶�
D. ���岻�ȶ������ú����ײ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������C��һ��ҽҩ�м��壬��ͨ�����з����ϳɣ�
��1��A�к��������ŵ�����Ϊ�� ��
��2��B�Ľṹ��ʽΪ ��
��3��B��C�ķ�Ӧ����Ϊ ��
��4��C��ͬ���칹��D�ܷ���������Ӧ������FeCl3��Һ������ɫ��Ӧ����1molD�������2molNaOH��Ӧ��D��������4�ֲ�ͬ��ѧ�������⣮��д��D��һ�ֽṹ��ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ˮ����Һ�����Ե���
A. NaClB. NaHCO3C. Na2OD. NaHSO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����14�֣�ij����ャҺ����Al��OH��3��MnO2������Na2CrO4 �� ���ǵ��������������ʹNa2CrO4������ȫ��ˮ������ij�о�С��������Ƶĵ�����װ�ã���ͼ����ʹ��Һ����ɹ�������ͺ���Ԫ����Һ�����������ã��ش��͢��е����⣮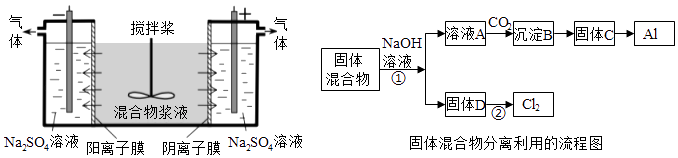
��������ķ�������ã�����ͼ�еIJ��ַ�������ͷ�Ӧ����δ������
��1����Ӧ�������Լ�NaOH�ĵ���ʽΪ �� B��C�ķ�Ӧ����Ϊ �� C��Al���Ʊ�������Ϊ ��
��2����С��̽����Ӧ�ڷ�����������D��Ũ�����ϣ������ȣ��ޱ仯��������Cl2���ɣ�����Ӧֹͣ������ʣ�࣬��ʱ�μ����ᣬ�ֲ���Cl2 �� �ɴ��ж�Ӱ��÷�Ӧ��Ч���е������У�����ţ� ��
a���¶� b��Cl����Ũ�� c����Һ�����
��3��0.1mol Cl2�뽹̿��TiO2��ȫ��Ӧ������һ�ֻ�ԭ�������һ����ˮ���TiO2xH2O��Һ̬���������4.28kJ���÷�Ӧ���Ȼ�ѧ����ʽΪ ��
��Ԫ����Һ�ķ��������
��4���ö��Ե缫���ʱ��CrO42���ܴӽ�Һ�з��������ԭ���� �� �����Ԫ�ص������������������ɵ�����Ϊ��д��ѧʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����100mLij���ʵ���Ũ�ȵ�NaOH��Һ�л���ͨ��һ������CO2 �� ��ַ�Ӧ����������Һ����ε���1mol/L��������Һ������������������״̬������������������ϵ��ͼ��ʾ 
��1��д��OA�η�����Ӧ�����ӷ���ʽ�� ��
��2����Ӧ��B��ʱ������Һ�е������� ��
��3��ԭNaOH��Һ�����ʵ���Ũ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȫ��̬����������ܶȸߡ��ɱ��ͣ��乤��ԭ����ͼ��ʾ�����е缫a���ò���ʯīϩ��S8���ϣ���ط�ӦΪ��16Li+xS8=8Li2Sx��2��x��8��������˵��������ǣ�������
A.��ع���ʱ�������ɷ�����Ӧ��2Li2S6+2Li++2e��=3Li2S4
B.��ع���ʱ�����·������0.02 mol���ӣ��������ϼ���0.14 g
C.ʯīϩ��������Ҫ����ߵ缫a�ĵ�����
D.��س��ʱ��Խ��������е�Li2S2��Խ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����У��������ȷ�Ӧ����
A. �ɱ�����B. ��ʯ������ˮ
C. ���������������Һ���D. Ba(OH)2��8H2O ��NH4Cl��Ͻ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������£��������绯ѧ��ʴ���� (����)
A.�����ڳ�ʪ�Ŀ�����
B.��������ˮ��
C.ͭ���ڵ���ˮ��
D.������ڳ�ʪ�Ŀ�����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com