
【题目】硫代硫酸钠可作为脱氯剂,已知25.0 mL 0.100 mol·L-1 Na2S2O3溶液恰好把112 mL Cl2(标准状况下)完全转化为Cl-离子,则S2O32-将转化成
A.SO42-B.SO32-C.SD.S2-
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】已知胆矾溶于水时溶液温度降低,胆矾分解的热化学方程式为:CuSO45H2O(s)=CuSO4(s)+5H2O(l) ΔH=+Q1kJ·mol-1;室温下,若将1 mol无水硫酸铜溶解为溶液时放热Q2kJ,则()
A. Q1>Q2 B. Q1=Q2 C. Q1<Q2 D. 无法比较
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组欲用化学方法测量一个不规则容器的体积,把40 g NaOH放入烧杯中,加入一定量的蒸馏水。待NaOH完全溶解后,将溶液全部转移到容器中,用蒸馏水稀释至完全充满容器,从中取出溶液100 mL,该溶液恰好与20mL 1mol/L CuSO4溶液完全反应。
(1)写出CuSO4的摩尔质量______________。
(2)求配制的NaOH溶液的物质的量浓度______________。
(3)试计算该容器的体积______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】支撑海港码头基础的钢管柱,常用外加电流的阴极保护法进行防腐,工作原理如图所示,其中高硅铸铁为惰性辅助阳极。下列有关表述不正确的是
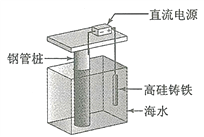
A. 通入保护电流使钢管桩表面腐蚀电流接近于零
B. 通电后外电路电子被强制从高硅铸铁流向钢管桩
C. 高硅铸铁的作用是作为损耗阳极材料和传递电流
D. 通入的保护电流应该根据环境条件变化进行调整
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合金贮氢材料具有优异的吸收氢性能,在配合氢能的开发中起到重要作用。
(1)一定温度下,某贮氢合金(M)的贮氢过程如图所示,纵轴为平衡时氢气的压强(p),横轴表示固相中氢原子与金属原子的个数比(H/M)。
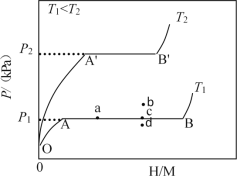
在OA段,氢溶解于M中形成固溶体MHx,随着氢气压强的增大,H/M逐惭增大;在AB段,MHx与氢气发生氢化反应生成氢化物MHy,氢化反应方程式为:zMHx(s)+H2(g)=ZMHy(s)△H(Ⅰ);在B点,氢化反应结束,进一步增大氢气压强,H/M几乎不变。反应(Ⅰ)中z=___(用含x和y的代数式表示)。温度为T1时,2g某合金4min内吸收氢气240mL,吸氢速率v=___mLg-1min。反应的焓变△H1__0(填“>”“<”或“=”)。
(2)η表示单位质量贮氢合金在氢化反应阶段的最大吸氢量占其总吸氢量的比例,则温度为T1、T2时,η(T1)____η(T2)(填“>”“<”或“=”)。当反应(Ⅰ)处于图中a点时,保持温度不变,向恒容体系中通入少量氢气,达到平衡后反应(Ⅰ)可能处于图中的___点(填“b”“c”或“d”),该贮氢合金可通过___或___的方式释放氢气。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高血脂严重影响人体健康,化合物E是一种临床治疗高血脂症的药物。E的合成路线如下(部分反应条件和试剂略):
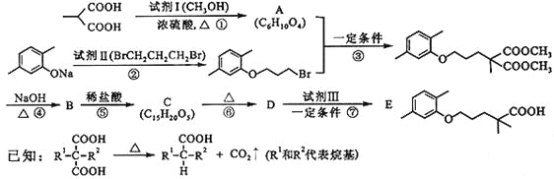
请回答下列问题:
(1)试剂Ⅰ的名称是___a___,试剂Ⅱ中官能团的名称是___b___,第② 步的反应类型是____c___。
(2)第①步反应的化学方程式是_____________。
(3)第⑥步反应的化学方程式是_____________。
(4)第⑦步反应中,试剂Ⅲ为单碘代烷烃,其结构简式是_________ 。
(5)C的同分异构体在酸性条件下水解,生成X、Y和CH3(CH2)4OH。若X含有羧基和苯环,且X和Y的核磁共振氢谱都只有两种类型的吸收峰,则X与Y发生缩聚反应所得缩聚物的结构简式是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸钠俗称纯碱,在日常生活和生活中有着广泛的应用.某化学兴趣小组想根据所学知识模拟制备碳酸钠,方法如下:先以NaCl、NH3、CO2和水等为原料以及下图所示装置制取NaHCO3(反应的化学方程式为NH3 + CO2 + H2O + NaCl = NaHCO3↓+ NH4Cl),然后再将NaHCO3制成Na2CO3。

(1)装置乙的作用是_________。为防止污染空气,尾气中含有的_________需要进行吸收处理。
(2)由装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有______、_______、____。NaHCO3转化为Na2CO3的化学方程式为_____________。
(3)若在(2)中反应时间较短,NaHCO3将分解不完全,该小组对一份加热了t1 min的NaHCO3样品的组成进行了以下探究:取加热了t1 min的NaHCO3样品27.4g完全溶于水制成溶液,然后向此溶液中不断滴加1mol·L-1的稀盐酸直到不再产生气泡,共消耗400 mL稀盐酸。请回答下列问题:
①根据实验的需要,用密度为1.19g ·cm-3 质量分数为36.5%的浓盐酸配制1mol·L-1的稀盐酸时,主要用到的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管和____(填仪器名称);需要量取的浓盐酸体积为:_____mL。
② 该样品中NaHCO3和Na2CO3的物质的量之比是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相对分子质量为M的气态化合物V L(标准状况),溶于m g 水中(不与水反应),得到质量分数为w%的溶液,物质的量浓度为cmol/L,密度为ρ g·cm-3,则下列说法正确的是
A. 溶液密度ρ= ![]() B. 相对分子质量M=
B. 相对分子质量M=![]()
C. 物质的量浓度c=![]() D. 溶质的质量分数w%=
D. 溶质的质量分数w%=![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
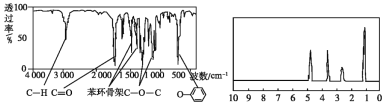
【题目】化合物A的相对分子质量为136,其红外光谱和核磁共振氢谱如图,下列关于A的说法中正确的是( )
A. 若A可水解,与其同类的化合物![]() 包括
包括![]() 的同分异构体只有5种
的同分异构体只有5种
B. 符合题中A分子结构特征的有机物类型可能不只1类
C. A的可能结构中在一定条件下最多可与![]() 发生加成反应
发生加成反应
D. A一定属于酯类化合物,在一定条件下能发生水解反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com