
| A、乙烯和乳酸(C3H6O3) |
| B、甲醛和葡糖糖 |
| C、乙烯和环己烷 |
| D、乙炔和苯 |
| 32 |
| 28 |
| 96 |
| 90 |


科目:高中化学 来源: 题型:
| 甲 | 乙 | |
| 丙 | 丁 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、35.5a=(w2-w1 )V2 | ||
B、n(Al)>
| ||
C、n(Na)+3n(Al)=
| ||
D、aV2=
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH4和CH3CH3 |
| B、CH3-CH2-Cl和CH2Cl-CH2Cl |
| C、CH2=CHCH2CH3和CH3CH=CHCH3 |
D、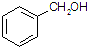 和 和 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:2:3 |
| B、2:1:6 |
| C、2:1:3 |
| D、1:2:6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、PM2.5的产生与人类活动无关 |
| B、在涂料中尽量用液态有机物代替水作溶剂,以减少环境污染 |
| C、酒精可使蛋白质变性,故能消毒杀菌 |
| D、塑化剂是一种化工塑料添加剂,可以大量添加到婴幼儿玩具中 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com