
”¾ĢāÄæ”æÓĆ50mL0.50mol/L ŃĪĖįÓė50 mL0.55mol/LNaOHČÜŅŗ£¬ŌŚÓŅĶ¼×°ÖĆÖŠ½ųŠŠÖŠŗĶČČµÄ²ā¶Ø£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
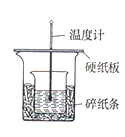
(1)“ÓŹµŃé×°ÖĆæ“£¬Ķ¼ÖŠÉŠČ±ÉŁµÄŅ»ÖÖ²£Į§ÓĆĘ·ŹĒ________”£
(2)ŌŚ²Ł×÷ÕżČ·µÄĒ°ĢįĻĀ£¬ĢįøßÖŠŗĶČČ²ā¶Ø×¼Č·ŠŌµÄ¹Ų¼üŹĒ________”£
(3)×ö1“ĪĶźÕūµÄÖŠŗĶČČ²ā¶ØŹµŃ飬ĪĀ¶Č¼ĘŠčŹ¹ÓĆ________“Ī£¬Ä³Ķ¬Ń§ĪŖĮĖŹ”Č„ĒåĻ“ĪĀ¶Č¼ĘµÄĀé·³£¬½ØŅ鏵Ń鏱Ź¹ÓĆĮ½Ö§ĪĀ¶Č¼Ę·Ö±š²āĮæĖįŗĶ¼īµÄĪĀ¶Č£¬ÄćŹĒ·ńĶ¬ŅāøĆĶ¬Ń§µÄ¹Ūµć£¬ĪŖŹ²Ć“£æ________”£
(4)ijĶ¬Ń§ŹµŃé¼ĒĀ¼Źż¾ŻČēĻĀ±ķĖłŹ¾¼ŁÉčŃĪĖįŗĶĒāŃõ»ÆÄĘČÜŅŗµÄĆܶȶ¼ŹĒ1g/mL£¬ÓÖÖŖÖŠŗĶ·“Ó¦ŗóÉś³ÉČÜŅŗµÄ±ČČČČŻc=4.18J/(g.”ę)øł¾ŻøĆĶ¬Ń§µÄŹµŃ鏿¾Ż¼ĘĖć£¬øĆŹµŃé²āµÄÖŠŗĶČČ”÷H=________”£
ĪĀ¶Č ŹµŃé“ĪŹż | ĘšŹ¼ĪĀ¶Čt1/”ę | ÖÕÖ¹ĪĀ¶Č t2/”ę | |||
HCl | NaOH | ||||
1 | 20.0 | 20.1 | 23.2 | ||
2 | 20.2 | 20.4 | 23.4 | ||
3 | 20.5 | 20.6 | 23.6 | ||
”¾“š°ø”æ»·ŠĪ²£Į§½Į°č°ō ±£ĪĀ 3“Ī ²»Ķ¬Ņā£¬ŅņĪŖ²»Ķ¬µÄĪĀ¶Č¼ĘĪó²ī²»Ķ¬ -51.8 kJ/mol
”¾½āĪö”æ
(1)øł¾ŻÖŠŗĶČČµÄ²ā¶ØŌĄķ·ÖĪö£»øł¾ŻĮæČČ¼ĘµÄ¹¹ŌģĄ“ÅŠ¶ĻøĆ×°ÖĆȱɣµÄŅĒĘ÷£»
(2)ÖŠŗĶČČ²ā¶ØŹµŃé³É°ÜµÄ¹Ų¼üŹĒ±£ĪĀ¹¤×÷£»
(3)²ā¶ØÖŠŗĶČČŅŖ²ā¶Ø·“Ó¦Ē°ŗóČÜŅŗµÄĪĀ¶Č£¬²»Ķ¬µÄŅĒĘ÷Īó²ī·¶Ī§²»Ķ¬£»
(4)ĻČøł¾Ż±ķÖŠ²ā¶ØŹż¾Ż¼ĘĖć³ö»ģŗĻŅŗ·“Ó¦Ē°ŗóµÄĘ½¾łĪĀ¶Č²ī£¬ŌŁøł¾ŻQ=cm”÷T¼ĘĖć³ö·“Ó¦·Å³öµÄČČĮ棬×īŗóøł¾ŻÖŠŗĶČȵÄŗ¬Ņå¼ĘĖć³öÖŠŗĶČČ”£
(1)ÖŠŗĶČČ²ā¶ØŹµŃé³É°ÜµÄ¹Ų¼üŹĒ±£ĪĀ¹¤×÷£¬ÄŚĶāÉÕ±ŅŖŅ»Ńłøߣ¬·ńŌņ£¬ČČĮæÉ¢Ź§“ó£»ÓÉĮæČČ¼ĘµÄ¹¹ŌģæÉÖŖøĆ×°ÖƵÄȱɣŅĒĘ÷ŹĒ»·ŠĪ²£Į§½Į°č°ō£»
(2)ÖŠŗĶČČ²ā¶ØŹµŃé³É°ÜµÄ¹Ų¼üŹĒ±£ĪĀ¹¤×÷£¬“óŠ”ÉÕ±Ö®¼äĢīĀśĖéÖ½Ģõ£¬ŌŚÉÕ±ÉĻ²æøĒÉĻÓ²ÖŹ°å£¬ÕāŃł¾ĶæÉŅŌ¼õÉŁŹµŃé¹ż³ĢÖŠµÄČČĮæĖšŹ§£»
(3)²ā¶ØÖŠŗĶČČŅŖ²ā¶Ø·“Ó¦Ē°ŃĪĖį”¢NaOHČÜŅŗµÄĪĀ¶Č¼°¶žÕß»ģŗĻŗóĒ”ŗĆĶźČ«·“Ó¦Ź±ČÜŅŗµÄĪĀ¶Č£¬¹Ź×ö1“ĪĶźÕūµÄÖŠŗĶČČ²ā¶ØŹµŃ飬ĪĀ¶Č¼ĘŠčŹ¹ÓĆ3“Ī£¬Ä³Ķ¬Ń§ĪŖĮĖŹ”Č„ĒåĻ“ĪĀ¶Č¼ĘµÄĀé·³£¬½ØŅ鏵Ń鏱Ź¹ÓĆĮ½Ö§ĪĀ¶Č¼Ę·Ö±š²āĮæĖįŗĶ¼īµÄĪĀ¶Č£¬ÓÉÓŚ²»Ķ¬µÄĪĀ¶Č¼ĘĪó²ī²»Ķ¬£¬ĖłŅŌøĆĶ¬Ń§µÄ¹Ūµć²»ŗĻĄķ£»
µŚ1“ĪŹµŃéŃĪĖįŗĶNaOHČÜŅŗĘšŹ¼Ę½¾łĪĀ¶ČĪŖ20.05”ę£¬·“Ó¦ŗóĪĀ¶ČĪŖ£ŗ23.2”ę£¬·“Ó¦Ē°ŗóĪĀ¶Č²īĪŖ3.15”ę£»
µŚ2“ĪŹµŃéŃĪĖįŗĶNaOHČÜŅŗĘšŹ¼Ę½¾łĪĀ¶ČĪŖ20.3”ę£¬·“Ó¦ŗóĪĀ¶ČĪŖ£ŗ23.4”ę£¬·“Ó¦Ē°ŗóĪĀ¶Č²īĪŖ3.1”ę£»
µŚ3“ĪŹµŃéŃĪĖįŗĶNaOHČÜŅŗĘšŹ¼Ę½¾łĪĀ¶ČĪŖ20.55”ę£¬·“Ó¦ŗóĪĀ¶ČĪŖ£ŗ23.6”ę£¬·“Ó¦Ē°ŗóĪĀ¶Č²īĪŖ£ŗ3.05”ę£»
Ę½¾łĪĀ¶Č²ī”÷T=£Ø3.15+3.1+3.05£©”ę”Ā3=3.1”ę£¬50mL 0.50mol/LŃĪĖįÓė50mL0.55mol/LNaOHČÜŅŗµÄÖŹĮæŗĶĪŖm=100mL”Į1g/cm3=100g£¬c=4.18J/(g”ę)£¬“śČė¹«Ź½Q=cm”÷TµĆÉś³É0.05molµÄĖ®·Å³öČČĮæQ=4.18J/(g”ę)”Į100g”Į3.1”ę=1.2958kJ£¬·“Ӧɜ³ÉH2OµÄĪļÖŹµÄĮæŅŌ²»×ćĮæµÄŃĪĖįĪŖ±ź×¼¼ĘĖć£¬n(H2O)=cV=0.50mol/L”Į0.05L=0.025mol£¬ĖłŅŌÖŠŗĶČČ”÷H=-![]() =-51.8kJ/mol”£
=-51.8kJ/molӣ


 ¾ŁŅ»·“Čżµ„ŌŖĶ¬²½¹ż¹Ų¾ķĻµĮŠ“š°ø
¾ŁŅ»·“Čżµ„ŌŖĶ¬²½¹ż¹Ų¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ£ŗN2(g)£«3H2(g) ![]() 2 NH3(g) ¦¤H£½£92.4 kJ”¤mol£1”£Ņ»¶ØĢõ¼žĻĀ£¬ĻÖÓŠČŻ»żĻąĶ¬ĒŅŗćČŻµÄĆܱÕČŻĘ÷¼×ÓėŅŅ£ŗ¢Ł Ļņ¼×ÖŠĶØČė1 mol N2ŗĶ3 mol H2£¬“ļµ½Ę½ŗāŹ±·Å³öČČĮæQ1 kJ£»¢Ś ĻņŅŅÖŠĶØČė0.5 mol N2ŗĶ1.5 mol H2£¬“ļµ½Ę½ŗāŹ±·Å³öČČĮæQ2 kJ”£ŌņĻĀĮŠ¹ŲĻµŹ½ÕżČ·µÄŹĒ
2 NH3(g) ¦¤H£½£92.4 kJ”¤mol£1”£Ņ»¶ØĢõ¼žĻĀ£¬ĻÖÓŠČŻ»żĻąĶ¬ĒŅŗćČŻµÄĆܱÕČŻĘ÷¼×ÓėŅŅ£ŗ¢Ł Ļņ¼×ÖŠĶØČė1 mol N2ŗĶ3 mol H2£¬“ļµ½Ę½ŗāŹ±·Å³öČČĮæQ1 kJ£»¢Ś ĻņŅŅÖŠĶØČė0.5 mol N2ŗĶ1.5 mol H2£¬“ļµ½Ę½ŗāŹ±·Å³öČČĮæQ2 kJ”£ŌņĻĀĮŠ¹ŲĻµŹ½ÕżČ·µÄŹĒ
A. Q1£½2Q2£½92.4B. 92.4£½Q1£¼2Q2
C. 92.4£¾Ql£¾2Q2D. Q1£½2Q2£¼92.4
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆĻĀĶ¼ĖłŹ¾×°ÖĆ½ųŠŠĻĀĮŠŹµŃé£ŗ½«¢ŁÖŠČÜŅŗµĪČė¢ŚÖŠ£¬Ō¤²āµÄĻÖĻóÓėŹµ¼ŹĻą·ūµÄŹĒ
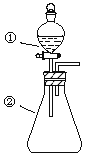
Ń”Ļī | ¢ŁÖŠĪļÖŹ | ¢ŚÖŠĪļÖŹ | Ō¤²ā¢ŚÖŠµÄĻÖĻó |
A | Ļ”ŃĪĖį | Ģ¼ĖįÄĘÓėĒāŃõ»ÆÄʵĻģŗĻČÜŅŗ | Į¢¼“²śÉśĘųÅŻ |
B | ÅØĻõĖį | ÓĆÉ°Ö½“ņÄ„¹żµÄĀĮĢõ | ²śÉśŗģ×ŲÉ«ĘųĢå |
C | ŠĀÖĘĀČĖ® | µķ·Ūµā»Æ¼ŲČÜŅŗ | ČÜŅŗ±äĄ¶É« |
D | ÅØŃĪĖį | MnO2 | ²śÉś»ĘĀĢÉ«ĘųĢå |
A.AB.BC.CD.D
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŹŅĪĀĻĀÓĆ![]() ·Ö±šµĪ¶Ø
·Ö±šµĪ¶Ø![]() µÄŃĪĖįŗĶ“×ĖįµÄĒśĻßČēĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
µÄŃĪĖįŗĶ“×ĖįµÄĒśĻßČēĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ

A.¢ń±ķŹ¾µÄŹĒµĪ¶ØŃĪĖįµÄĒśĻß
B.![]() Ź±£¬Į½·ŻČÜŅŗÖŠ£ŗ
Ź±£¬Į½·ŻČÜŅŗÖŠ£ŗ![]()
C.![]() Ź±£¬Į½·ŻČÜŅŗÖŠ£ŗ
Ź±£¬Į½·ŻČÜŅŗÖŠ£ŗ![]()
D.![]() Ź±£¬“×ĖįČÜŅŗÖŠ£ŗ
Ź±£¬“×ĖįČÜŅŗÖŠ£ŗ![]()
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŃĒĢśĒč»Æ¼Ų¾§Ģå»ÆѧŹ½ĪŖ£ŗKxFey(CN)znH2O£¬Ė×³Ę»ĘŃŖŃĪ£¬³£ÓĆ×÷Ź³Ę·æ¹½į¼Į”£Ņ»ÖÖÓĆNaCN£ØNĻŌ-3¼Ū£©·ĻŅŗÖĘČ”»ĘŃŖŃĪµÄÖ÷ŅŖ¹¤ŅÕĮ÷³Ģ£ŗ
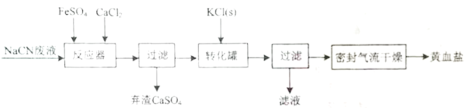
£Ø1£©ŹµŃéŹŅÓĆĀĢ·Æ¹ĢĢåÅäÖĘFeSO4ČÜŅŗŹ±£¬Ó¦ĻČ________£¬ŌŁÓĆÕōĮóĖ®Ļ”ŹĶ”£
£Ø2£©”°×Ŗ»Æ¹Ž”±ÖŠÉś³É»ĘŃŖŃĪ¾§ĢåµÄ·“Ó¦ĄąŠĶĪŖ________”£
£Ø3£©²ÉÓĆĆÜ·āĘųĮ÷øÉŌļČ”“śŌŚĶØ·ē³÷ÄŚøÉŌļµÄŌŅņŹĒ________”£
£Ø4£©»ĘŃŖŃĪµÄ»ÆѧŹ½æÉĶعżĻĀĮŠŹµŃé²ā¶Ø£ŗ
¢Ł×¼Č·³ĘČ”4.220gѳʷ¼ÓČėĖ®ÖŠ³ä·ÖČܽā£¬½«ĖłµĆČÜŅŗ×ŖŅĘÖĮČŻĮæĘæÅäÖĘ³É100.00mLČÜŅŗA”£
¢ŚĮæČ”25.00mLČÜŅŗA£¬ÓĆ2.000molL-1KMnO4ČÜŅŗµĪ¶Ø£¬“ļµ½µĪ¶ØÖÕµćŹ±£¬¹²ĻūŗÄKMnO4ČÜŅŗ15.25mL”£·“Ó¦ČēĻĀ£ØĪ“ÅäĘ½£©£ŗ![]() ¢ŪĻņ¢ŚĖłµĆČÜŅŗ¼ÓČėMn2+Ąė×Ó½»»»Ź÷Ö¬£¬½«Mn2+ĶźČ«Īüø½ŗóŌŁµĪ¼Ó×ćĮæNaOHČÜŅŗ£¬¹żĀĖ”¢Ļ“µÓ”¢×ĘÉÕ£¬×īÖÕµĆ¹ĢĢå0.2g”£
¢ŪĻņ¢ŚĖłµĆČÜŅŗ¼ÓČėMn2+Ąė×Ó½»»»Ź÷Ö¬£¬½«Mn2+ĶźČ«Īüø½ŗóŌŁµĪ¼Ó×ćĮæNaOHČÜŅŗ£¬¹żĀĖ”¢Ļ“µÓ”¢×ĘÉÕ£¬×īÖÕµĆ¹ĢĢå0.2g”£
Ķعż¼ĘĖćČ·¶ØѳʷµÄ»ÆѧŹ½£ØŠ“³ö¼ĘĖć¹ż³Ģ£©”£______________
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ ClO2ŹĒŅ»ÖÖĒæŃõ»ÆŠŌĘųĢ壬ŌŚĻū¶¾ŗĶ¹ūŹß±£ĻŹµČ·½ĆęÓ¦ÓĆ¹ć·ŗ”£Ä³ŠĖȤŠ”×éĶعżČēĶ¼ĖłŹ¾×°ÖƶŌĘä½ųŠŠÖʱø”¢ŹÕ¼Æ”¢ĪüŹÕ²¢ÖĘČ”NaClO2”£

£Ø1£©ŅĒĘ÷AµÄĆū³ĘŹĒ________”£
£Ø2£©Ķ¼ÖŠ×°ÖĆÓŠŅ»Ć÷ĻŌ“ķĪó£¬ĒėÖø³ö£ŗ________”£
£Ø3£©“ņæŖBµÄ»īČū£¬AÖŠÓŠClO2Éś³É£¬DÖŠĪüŹÕClO2ŗóÉś³ÉNaClO2ŗĶNaHCO3£¬Š“³öDÖŠĖł·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ________”£
£Ø4£©EÖŠČÜŅŗ³öĻÖ»ĘÉ«ÄÜ·ńĖµĆ÷ClO2Ī“±»H2O2ŗĶNa2CO3µÄ»ģŗĻČÜŅŗ³ä·ÖĪüŹÕ£¬ÅŠ¶Ļ²¢ĖµĆ÷ĄķÓÉ£ŗ________”£
£Ø5£©Š“³öŅ»ÖÖĢįøßClO2ĪüŹÕĀŹµÄ·½·Ø£ŗ________”£
£Ø6£©E×°ÖĆĪüŹÕŅŻ³öµÄÉŁĮæClO2ĘųĢåŗóĖłµĆČÜŅŗ£ØpHĪŖ5.5~6.5£©ÖŠ“ęŌŚÉŁĮæClO2-£¬µ±pH”Ü2Ź±£¬ClO2-Äܱ»I»¹Ō”£Ēė²¹³äĶźÕū¼ģŃéE×°ÖĆČÜŅŗÖŠ“ęŌŚÉŁĮæClO2-µÄŹµŃé·½°ø£ŗČ”Ņ»¶ØĢå»żE×°ÖĆÖŠµÄČÜŅŗÓŚ·ÖŅŗĀ©¶·ÖŠ£¬________£¬ŌņČÜŅŗÖŠ“ęŌŚClO2-”££ØŹµŃéÖŠŠėŹ¹ÓƵďŌ¼ĮÓŠ£ŗCCl4”¢Ļ”ĮņĖį”¢µķ·ŪČÜŅŗ£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æA”ŖJŹĒ֊ѧ»Æѧ֊³£¼ūµÄĪļÖŹ£¬ĖüĆĒÖ®¼äµÄ×Ŗ»Æ¹ŲĻµČēĻĀæņĶ¼ĖłŹ¾£Ø²æ·Ö²śĪļŅŃĀŌČ„£©”£ŅŃÖŖAŹĒŅ»ÖÖøßČŪµćĪļÖŹ£¬JŹĒŅ»ÖÖŗģŗÖÉ«³Įµķ”£
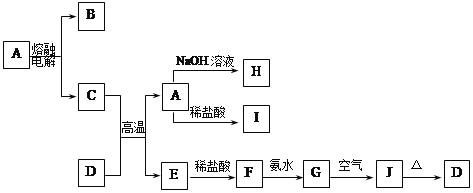
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©AµÄ»ÆѧŹ½ĪŖ_______£¬ŌŚĖ®ÖŠµÄČܽāŠŌ_____£ØŃ”Ģī”°Ņ×ČÜ”±”¢”°æÉČÜ”±”¢”°ÄŃČÜ”±£©”£
£Ø2£©HČÜŅŗÖŠĶØČė¹żĮæµÄCO2£¬Ęä·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ____________________”£
G”śJµÄ»Æѧ·½³ĢŹ½ĪŖ___________________________________________”£
·“Ó¦µÄĻÖĻóŹĒ______________________________________________”£
£Ø3£©DĪļÖŹĒ”ŗĆČÜÓŚŅ»¶ØĮæµÄĻ”ŃĪĖįŗó£¬ÓĆŗĻŹŹµÄ»ÆѧÓĆÓļ±ķŹ¾ĖłµĆČÜŅŗĻŌĖįŠŌµÄŌŅņ___________________________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”ææØÄŖ·śGŹĒŅ»ÖÖæ¹Ö×ĮöŅ©,æØÄŖ·ś¾ßÓŠŅÖÖĘ²”¶¾ø“ÖʵĊ§¹ū.æÉÄÜÓĆÓŚÖĪĮĘøŠČ¾ŠĀŠĶ¹Ś×“²”¶¾µÄ»¼Õß”£GµÄŅ»ÖÖŗĻ³ÉĀ·ĻßČēĶ¼ĖłŹ¾£ŗ

ŅŃÖŖ£ŗ
¢ŁAF·Ö×ÓĢ¼Į“ÖŠ¾ł²»ŗ¬»·×“ŗĶÖ§Į“½į¹¹”£
¢ŚH-N=C=O+NH3”ś![]()
»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©AÖŠ¹ŁÄÜĶŵÄĆū³ĘĪŖ___________”£
£Ø2£©Š“³öBŗĶŅų°±ČÜŅŗ·“Ó¦µÄ»Æѧ·½³ĢŹ½___________”£
£Ø3£©C”śDµÄ·“Ó¦ĄąŠĶĪŖ___________”£
£Ø4£©FÓė5”ŖFU·“Ӧɜ³ÉæØÄŖ·śG£¬5Ņ»FUµÄ½į¹¹¼ņŹ½ĪŖ___________£¬GµÄ·Ö×ÓŹ½ĪŖ__________________________,
£Ø5£©F(C6H13N=C=O)µÄŅ»ÖÖĶ¬ĻµĪļH½į¹¹¼ņŹ½ĪŖC3H7N=C=O£¬HµÄĶ¬·ÖŅģ¹¹ĢåÖŠŗ¬½į¹¹![]() £¬µ«ŹĒ²»ŗ¬»·×“½į¹¹µÄ¹²ÓŠ___________Ö֣ز»°üĄØĮ¢ĢåŅģ¹¹£©£¬Š“³öŅ»ÖÖŗĖ“Ź²ÕńĒāĘ×ĪŖĪå×é·åµÄĶ¬·ÖŅģ¹¹Ģå½į¹¹¼ņŹ½___________”£
£¬µ«ŹĒ²»ŗ¬»·×“½į¹¹µÄ¹²ÓŠ___________Ö֣ز»°üĄØĮ¢ĢåŅģ¹¹£©£¬Š“³öŅ»ÖÖŗĖ“Ź²ÕńĒāĘ×ĪŖĪå×é·åµÄĶ¬·ÖŅģ¹¹Ģå½į¹¹¼ņŹ½___________”£
£Ø6£©DMF(N.N”Ŗ¶ž¼×»ł¼×õ£°·£©½į¹¹¼ņŹ½ĪŖ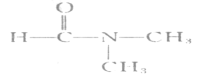 £¬ŹĒŅ»ÖÖÖŲŅŖµÄ»Æ¹¤ŌĮĻ¼°ČܼĮ”£ŅŃÖŖR-OH+NH3”śRNH2+H2O£»R”ŖCOOR”Æ+NH3”śRCONH2+R”ÆOH”£Š“³öŅŌCH3OHĪŖŌĮĻÖʱøDMFµÄŗĻ³ÉĀ·ĻߣØĪŽ»śŹŌ¼ĮČĪŃ”£©”£____________
£¬ŹĒŅ»ÖÖÖŲŅŖµÄ»Æ¹¤ŌĮĻ¼°ČܼĮ”£ŅŃÖŖR-OH+NH3”śRNH2+H2O£»R”ŖCOOR”Æ+NH3”śRCONH2+R”ÆOH”£Š“³öŅŌCH3OHĪŖŌĮĻÖʱøDMFµÄŗĻ³ÉĀ·ĻߣØĪŽ»śŹŌ¼ĮČĪŃ”£©”£____________
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潫3. 84 gĶ·ŪÓėŅ»¶ØÖŹĮæÅØĻõĖį·“Ó¦£¬µ±ĶĶźČ«×÷ÓĆŹ±£¬ČÜŅŗÖŠµÄNO3-¼õÉŁ0.1mol£¬ŌņĖłĻūŗÄĻõĖįµÄĪļÖŹµÄĮæŹĒ
A.0.1 molB.0.11 molC.0.16 molD.0.22 mol
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com