
【题目】下列各组物质中,互为同分异构体的是
A.CH3CH2CH3 和CH3CH(CH3)CH3B.CH3CH2OH 和 CH3CHO
C.CH3COOH 与 HCOOCH3D.![]() 和
和 ![]()
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】胆矾CuSO4·5H2O可写[Cu(H2O)4]SO4·H2O,其结构示意图如下:

下列有关胆矾的说法正确的是( )
A. Cu2+的价电子排布式为3d84s1
B. 所有氧原子都采取sp3杂化
C. 氧原子参与形成离子键、配位键和氢键三种化学键
D. 胆矾中的水在不同温度下会分步失去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组同学欲在实验室中用乙醇制备1,2-二溴乙烷。
甲同学设计的实验装置如下图:
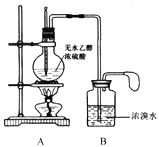
(1)请写出A和B中发生的主要反应的化学方程式
A:________________________________________。
B:________________________________________。
(2)乙同学查阅资料得知:
①此反应可能存在的主要副反应有:在浓硫酸的存在下,乙醇可发生如下反应生成乙醚, ![]()
②乙醚不与溴水反应
有关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | |
颜色、状态 | 无色液体 | 无色液体 | 无色液体 |
沸点/℃ | 78.5 | 132 | 34.6 |
若最终产物中混有少量乙醚,可用__________的方法除去。
(3)丙同学观察到:在实验后期A中液体变黑,认为应该在装置A和B之间加入装置__________(填序号),此装置的作用是____________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某体积可变的密闭容器,盛有适量的A和B的混合气体,在一定条件下发生反应:![]() ,若维持温度和压强不变,当达到平衡时,容器的体积为VL,其中C的体积分数为
,若维持温度和压强不变,当达到平衡时,容器的体积为VL,其中C的体积分数为![]() ,下列推断中正确的是
,下列推断中正确的是![]()
①原混和气体的体积为![]()
②反应前气体A有![]()
③反应平衡时气体B消耗掉![]()
④平衡时B的体积分数为![]()
A.①③B.①④C.②③D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同温度下,体积为2L的两个恒容容器中发生:![]() 均为气态物质
均为气态物质![]() 有下表所示实验数据:
有下表所示实验数据:
容器编号 | 起始时各物质的物质的量 | 达到平衡时体系能量的变化 | ||
|
|
| ||
① | 1 | 3 | 0 |
|
② | 0 | 0 | 2 |
|
③ |
|
|
|
|
下列有关说法正确的是
A.![]()
B.②中![]() 的转化率大于③中
的转化率大于③中![]() 的转化率
的转化率
C.容器①与③分别达到平衡时,平衡常数相同,且![]()
D.将容器①的反应条件换为恒温恒压中进行![]() 投料量不变
投料量不变![]() ,达到平衡时,气体平均摩尔质量较恒温恒容时减小了
,达到平衡时,气体平均摩尔质量较恒温恒容时减小了
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】.在一定体积和一定条件下有反应N2(g)+3H2(g)![]() 2NH3(g),现分别从两条途径建立平衡:
2NH3(g),现分别从两条途径建立平衡:
Ⅰ.起始浓度N2:1 mol·L-1,H2:3 mol·L-1
Ⅱ.起始浓度N2:2 mol·L-1,H2:6 mol·L-1
则下列叙述正确的是( )
A. Ⅰ和Ⅱ两途径达到平衡时,体系内各成分的体积分数相同
B. 达到平衡时,途径Ⅰ的反应速率v(H2)等于途径Ⅱ的反应速率v(H2)
C. 达到平衡时,途径Ⅱ体系内混合气体的压强是途径Ⅰ内混合气体压强的2倍
D. 达到平衡时,途径Ⅰ体系内混合气体的密度为途径Ⅱ体系内混合气体的密度的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.在密闭容器中进行下列反应:CO2(g)+C(s)![]() 2CO(g) ΔH>0,达到平衡后,若改变下列条件,则平衡如何移动?(填“向左移动”、“向右移动”或“不移动”)
2CO(g) ΔH>0,达到平衡后,若改变下列条件,则平衡如何移动?(填“向左移动”、“向右移动”或“不移动”)
(1)增加C(s),平衡___。
(2)减小密闭容器容积,保持温度不变,则平衡___。
(3)通入N2,保持密闭容器容积和温度不变,则平衡__。
(4)保持密闭容器容积不变,升高温度,则平衡__。
Ⅱ.在一密闭容器中发生下列反应:N2(g)+3H2(g)![]() 2NH3(g) ΔH<0,如图是某一时间段反应速率与反应进程的关系曲线图。
2NH3(g) ΔH<0,如图是某一时间段反应速率与反应进程的关系曲线图。

下列时间段中,氨的百分含量最高的是(_____)
A.0~t1 B.t2~t3
C.t3~t4 D.t4~t5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用质量分数为36.5%的浓盐酸(密度为1.16 g·cm-3)配制成1 mol/L的稀盐酸220 mL,试回答下列问题:
(1)配制稀盐酸时,应选用容量为________mL的容量瓶。
(2)经计算需要________mL浓盐酸,在量取时宜选用________量筒。
A.5 mL B.10 mL C.25 mL D.50 mL
(3)在量取浓盐酸后,进行了下列操作:
①等稀释的盐酸的温度与室温一致后,沿玻璃棒注入容量瓶中。
②往容量瓶中小心加蒸馏水至液面距容量瓶刻度线1~2 cm时,改用胶头滴管加蒸馏水,使溶液的液面与瓶颈的刻度标线相切。
③在盛盐酸的烧杯中注入蒸馏水,并用玻璃棒搅拌,使其混合均匀。
④用蒸馏水洗涤烧杯和玻璃棒2至3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是(填序号)________。
(4)在上述配制过程中,用刚刚洗涤洁净的量筒来量取浓盐酸,其配制的稀盐酸浓度会______(填“偏高”“偏低”或“无影响”)。若未用蒸馏水洗涤烧杯内壁和玻璃棒或未将洗涤液注入容量瓶,则配制的稀盐酸浓度会________(填“偏高”“偏低”或“无影响”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com