
| 滴定序号 | 待测液体积 (mL) | 所消耗盐酸标准液的体积(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.50 | 20.70 |
| 2 | 20.00 | 6.00 | 26.00 |
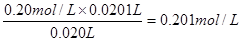 。所以样品的纯度是
。所以样品的纯度是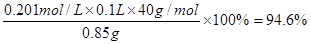 。
。

科目:高中化学 来源:不详 题型:单选题
| A.1:9 | B.1:11 | C.9:1 | D.11:1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.稀HCl和稀NaOH |
| B.1.0 mol·L-1 HCl和1.0 mol·L –1 NaOH |
| C.500 mL 2.0 mol·L-1 HCl和500 mL2.0 mol·L –1 NaOH |
| D.500 mL 2.0 mol·L-1 H2SO4和500 mL 2.0 mol·L-1 Ba(OH)2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.无论是纯水,还是酸性、碱性或中性稀溶液,在常温下,其c(H+)×c(OH-)=1×10-14 |
| B.c(H+)等于1×10-7 mol/L的溶液一定是中性溶液 |
| C.0.2 mol/L CH3COOH溶液中的c(H+)是0.1 mol/L CH3COOH溶液中的c(H+)的2倍 |
| D.强电解质的水溶液中不存在电解质分子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 滴定次数 | 盐酸体积 | NaOH溶液体积读数(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.00 | 18.10 |
| 2 | 20.00 | 0.00 | 16.30 |
| 3 | 20.00 | 0.00 | 16.22 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.滴定终点读数时,俯视滴定管的刻度,其它操作均正确; |
| B.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗; |
| C.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液; |
| D.未用标准液润洗碱式滴定管; |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com