
X、Y、Z、W 属于同周期的短周期主族元素,原子序数依次增大,它们的原子最外层电子数之和为17,且Y原子最外层电子数是X原子最外层电子数的3倍,W的内层电子数比最外层电子数多。下列说法正确的是
A.原子半径大小:r(X)>r(Y);简单离子半径大小:r(W)>r(Z)
B.X、Y、Z最高价氧化物的水化物两两之间可以发生反应
C.氢化物的稳定性:W>Z;氧化物水化物的酸性:W>Z
D.甲物质由Y和Z元素组成,溶于水后得到甲的水溶液
B
【解析】
试题分析:根据X、Y、Z、W 属于同周期的短周期主族元素,W的内层电子数比最外层电子数多,说明这四种元素为第三周期元素,Y原子最外层电子数是X原子最外层电子数的3倍,则X为Na元素、Y为Al元素,则Z、W的最外层电子数之和为13,则Z为S元素、W为Cl元素。A、简单离子半径大小,S2?半径大于Cl?半径,所以r(Z) > r(W),错误;B、X、Y、Z最高价氧化物的水化物分别为NaOH、Al(OH)3、H2SO4,Al(OH)3为两性氢氧化物,故两两之间可以发生反应,正确;C、没有指明氧化物水化物是否为最高价,酸性强弱无法比较,错误;D、甲物质由Y和Z元素组成,为Al2S3,溶于水后发生完全水解反应,得不到Al2S3溶液,错误。
考点:本题考查元素的推断、元素周期律、盐类的水解。


 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源:2013-2014学年广东省深圳市高三第二次调研考试理综化学试卷(解析版) 题型:选择题
NA为阿伏伽德罗常数。下列说法正确的是( )
A.同温同压同体积的CO2和SO2所含氧原子数均为2NA
B.32gCu与S完全反应转移的电子数为NA
C.1L 1.0mol·L-1NH4Cl与2L 0.5mol·L-1NH4Cl溶液含NH4+数目相同
D.25℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH-数目为0.1NA
查看答案和解析>>
科目:高中化学 来源:2013-2014学年广东省十校联考高三下学期理综化学试卷(解析版) 题型:填空题
(16分)香豆素(结构如下图中Ⅰ所示)是用途广泛的香料,由香豆素经下列图示的步骤可转变为水杨酸。
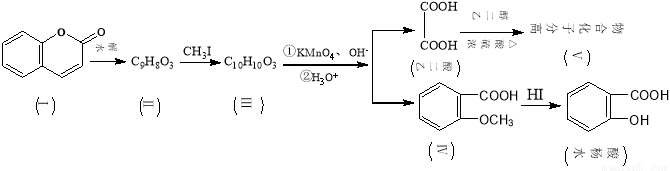 已知:CH3CH=CHCH2CH3
已知:CH3CH=CHCH2CH3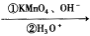 CH3COOH+CH3CH2COOH
CH3COOH+CH3CH2COOH
请回答下列问题:
(1)化合物Ⅱ分子中的含氧官能团的名称为 ,由乙二酸生成高分子化合物Ⅴ的反应类型为。
(2)下列关于有机物Ⅰ、Ⅱ、Ⅲ、Ⅳ的叙述中正确的是(选填编号)
A.1molⅠ最多能和5mol H2发生加成反应B.可用FeCl3溶液来鉴别Ⅱ和Ⅲ
C.Ⅳ中核磁共振氢谱共有4种峰 D.Ⅰ、Ⅱ、Ⅲ均可使溴的四氯化碳溶液褪色
(3)香豆素在过量NaOH溶液中完全水解的化学方程式为
(4)Ⅲ的结构简式为 ,在上述转化过程中,设计反应步骤Ⅱ→Ⅲ的目的是 。
(5)化合物Ⅳ有多种同分异构体,请写出其中一种符合下列条件的同分异构体的结构简式: 。
①是苯的对位二取代物;②水解后生成的产物之一能发生银镜反应。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年山东省枣庄市高三下学期第二次模拟考试理综化学试卷(解析版) 题型:选择题
下列叙述Ⅰ和Ⅱ均正确且有因果关系的是( )
选项 | 叙述Ⅰ | 叙述Ⅱ |
A | NH4Cl为强酸弱碱盐 | 用加热法除去NaCl中的NH4Cl |
B | 溶解度:CaCO3<Ca(HCO3)2 | 溶解度:Na2CO3<NaHCO3 |
C | SiO2与HF反应 | 氢氟酸不能保存在玻璃瓶中 |
D | Fe3+具有氧化性 | 用KSCN溶液可以鉴别Fe3+ |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年山东省文登市高三第三次统考理科综合化学试卷(解析版) 题型:选择题
已知水在25℃和95℃时,其电离平衡曲线如图所示,下列说法错误的
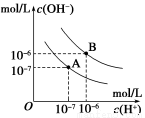
A.A曲线代表25℃时水的电离平衡曲线
B.当95℃时,pH=6的溶液呈中性
C.25℃时,将10mLpH=12的NaOH溶液与1mLpH=1的H2SO4 溶液混合,所得溶液的pH=7
D.95℃时,等体积等物质的量浓度的HA溶液和NaOH溶液混合后,当混合溶液的pH=6时,说明HA酸为弱酸
查看答案和解析>>
科目:高中化学 来源:2013-2014学年山东省德州市高三4月模拟考试(二模)理综化学试卷(解析版) 题型:填空题
镁、铝、铁及其化合物在生产、生活中有着广泛的应用
I:实验室采用MgCl2、AlCl3的混合溶液与过量氨水反应制备MgAl2O4,主要流程如下:
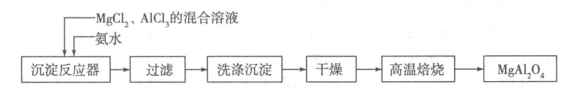
(1)已知25℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Al(OH)3]=3×10-34,该温度下向浓度均为0.01 mol·L-1的MgCl2和AlCl3混合溶液中逐滴加入氨水,先生成 沉淀(填化学式)。
(2)高温焙烧时发生反应的化学方程式 ,洗涤沉淀时的方法是 。
(3)常温下如果向AlCl3饱和溶液中不断通人HCl气体,可析出AlCl3·6H2O晶体,结合化学平衡移动原理解释析出晶体的原因: 。
Ⅱ:某兴趣小组的同学发现将一定量的铁与浓硫酸加热时,观察到铁完全溶解,并产生大量气体。为此,他们设计了如下装置验证所产生的气体。
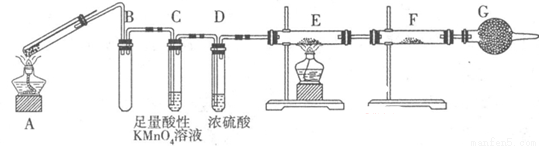
(1)G装置的作用是 。
(2)证明有SO2生成的现象是 ,为了证明气体中含有氢气,装置E和F中加入的试剂分别为 、 。
(3)若将铁丝换成铜丝,反应后的溶液没有出现预计的蓝色溶液,而出现了大量白色固体,原因是 。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年山东省德州市高三4月模拟考试(二模)理综化学试卷(解析版) 题型:选择题
下列有关叙述不正确的是
A.MgO、Al2O3熔点高,可用于制作耐火材料
B.用浓氢氧化钠溶液可除去乙酸乙酯中混有的乙酸、乙醇杂质
C.除去NaCl溶液中的Na2CO3,应选择试剂为盐酸,而不是硝酸
D.油脂在碱性条件下易发生水解,可用于制作肥皂
查看答案和解析>>
科目:高中化学 来源:2013-2014学年天津市七校高三4月联考理综化学试卷(解析版) 题型:选择题
常温下,用0.1000 mol·L-1 NaOH溶液分别滴定20.00 mL 0.1000 mol·L-1 盐酸和20.00 mL 0.1000 mol·L-1醋酸溶液,得到两条滴定曲线,如下图所示,若以HA表示酸,下列说法正确的是
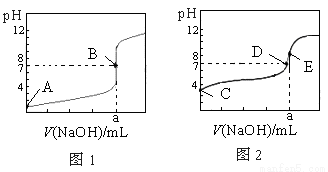
A.滴定盐酸的曲线是图2
B.达到B、E状态时,反应消耗的n(CH3COOH)>n(HCl)
C.达到B、D状态时,两溶液中离子浓度均为c(Na+)=c(A-)
D.当0 mL<V(NaOH)<20.00 mL时,对应混合液中各离子浓度大小顺序为c(A-)>c(Na+)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源:2013-2014学年北京市丰台区高三下学期统一练习(一)化学试卷(解析版) 题型:填空题
聚乙烯醇肉桂酸酯(A)可用于光刻工艺中做抗腐蚀涂层。下面是一种合成该有机物的路线:
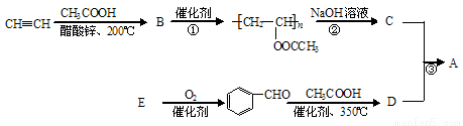
已知: 
请回答:
(1)CH3COOH中的含氧官能团的名称为 ;其电离方程式是______。
(2)反应①是加聚反应,B的结构简式是 。
(3)反应②的反应类型是 。
(4)E的分子式为C7H8O,符合下列条件的E的同分异构体的结构简式是 。
① 能与浓溴水反应产生白色沉淀 ②核磁共振氢谱有4种峰
(5) 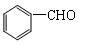 能与新制的Cu(OH)2反应,该反应的化学方程式是 。
能与新制的Cu(OH)2反应,该反应的化学方程式是 。
(6)关于D的性质下列说法正确的是 (填字母)。
a.存在顺反异构
b.溶液呈酸性,能与Na和NaOH溶液反应
c.能使KMnO4(H+)溶液和Br2(CCl4)溶液褪色
d.能发生银镜反应、酯化反应、加成反应和消去反应
(7)反应③的化学方程式是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com